Руководитель

д.х.н.
Беляева Ксения Васильевна
ведущий научный сотрудник
7 (3952) 42-55-85 (353)
Кадровый состав
Беляева Ксения Васильевна – главный научный сотрудник, д.х.н.
Колыванов Никита Александрович – старший научный сотрудник, к.х.н.
Никитина Лина Павловна – старший научный сотрудник, к.х.н.
Опарина Людмила Андреевна – старший научный сотрудник, к.х.н.
Салий Вероника Сергеевна – младший научный сотрудник, аспирант.

Направление (область) научных исследований и тематика
Создание оригинальных методологий направленного синтеза прекурсоров и аналогов лекарственных средств на основе каскадных мультимолекулярных однореакторных реакций высокоэлектрофильных ацетиленов с нейтральными нуклеофилами в присутствии оснований, с участием винильных цвиттер-ионов и их карбеновых интермедиатов, запускающих ранее неизвестные процессы функционализации и модификации фундаментальных азотистых гетероциклов.
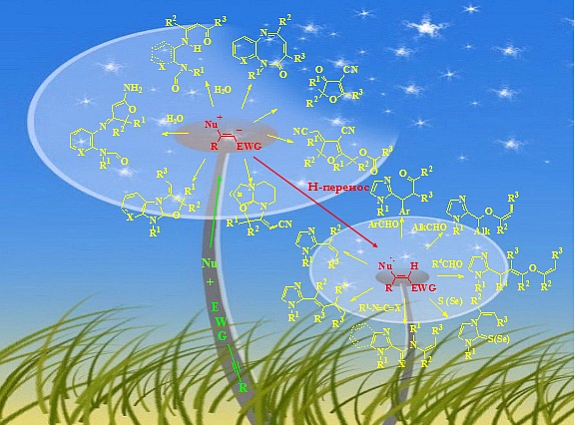
Основные научные результаты (фундаментальные исследования) за 2020-2024 гг.
1. Синтез фуро[3,4-b]хинолинонов и фуроиминохинолинов однореакторной реакцией 2,3-функционализации-циклизации хинолинов ацеталями цианопропаргиловых спиртов
Развитие 2,3-дифункционализации хинолинов под действием электронодефицитных ацетиленов на примере ацеталей цианопропаргиловых спиртов (KOH/H2O/MeCN, 55-60 oC) позволило получить соответствующие 2-(1-этоксиалкокси)-3-цианохинолины с выходами до 50%, которые при гидролизе (7% водный HCl, ацетон, 20-25 oC) количественно подвергаются легкой циклизации через фуро[3,4-b]иминохинолины в фуро[3,4-b]хинолиноны (до 98%).
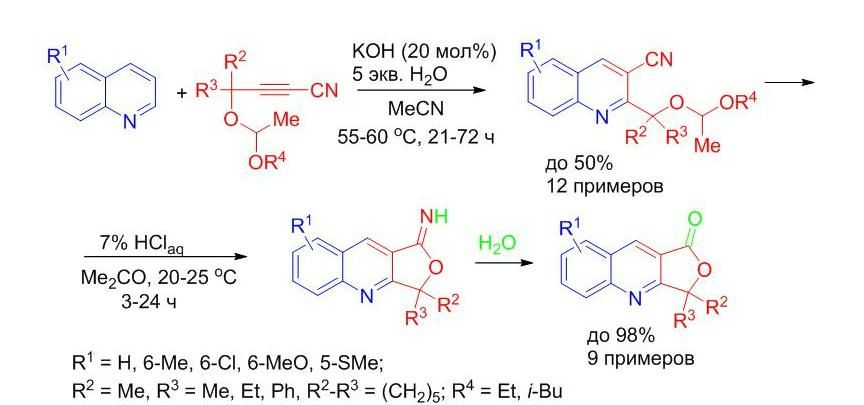
Показана возможность однореакторной реализации синтеза фуро[3,4-b]хинолинонов непосредственно из хинолинов и ацеталей цианопропаргиловых спиртов.
Belyaeva K.V., Nikitina L.P., Afonin A.V., Grishchenko L.A., Trofimov B.A. Cyanoquinolines and furo[3,4‑b]quinolinones formation via on-the-spot 2,3-functionalization of quinolines with cyanopropargylic alcohols // Journal of Organic Chemistry. – 2021. – V. 86. – Is. 5. – P. 3800-3809.
2. Арилоксалилацетилены как диэлектрофилы для аннелирования и функционализации азинов
Исследование реакционной способности малоизученного класса электронодефицитных ацетиленов – арилоксалилацетиленов, при взаимодействии с азинами позволило разработать атом-экономные, прямые, однореакторные подходы к глубоко функционализированным 1,3-оксазинам, аннелированным к пиридиновым, хинолиновым, изохинолиновым и фенантридиновым циклам. Показано, что в случае реакции между фенантридином и арилоксалилацетиленами, протекающей в воде, реализуется аннелирование по типу 1:1:1 с образованием гидроксизамещенного оксазинофенантридина, в то время как акридин под действием то же системы (арилоксалилацетилен/вода) приводит к продуктам N(1),С(9)-функционализации.
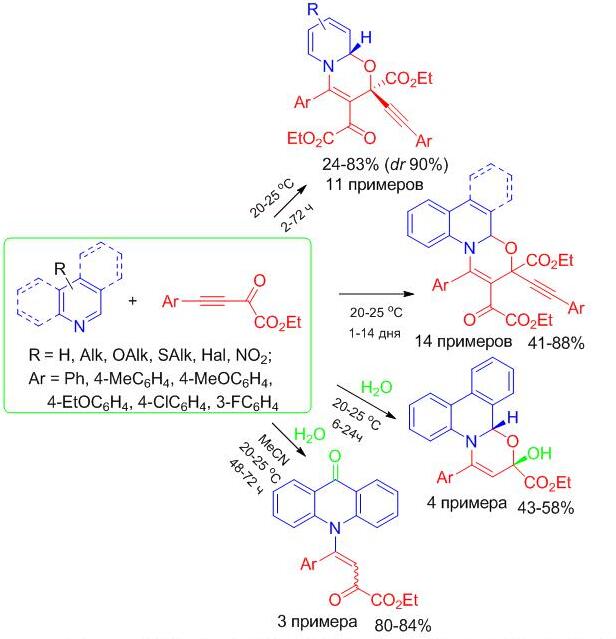
Belyaeva K.V., Gen’ V.S., Nikitina L.P., Afonin A.V., Pavlov D.V., Trofimov B.A. Uniquely functionalized tetrahydropyrido[2,1-b][1,3]oxazines: diastereoselective 1:2 assembly from pyridines with oxalylacetylenes // Tetrahedron Letters. – 2021. – V. 84. Atricle number 153431. DOI: 10.1016/j.tetlet.2021.153431
Belyaeva K.V., Gen’ V.S., Nikitina L.P., Afonin A.V., Trofimov B.A. Oxalylacetylenes as dielectrophiles for annulation of quinoline ring: synthesis of highly functionalized 1,3-oxazinoquinolines // Synthesis. – 2022. – V. 54. – N. 7. – P. 1833-1842. DOI: 10.1055/a-1644-2930
Belyaeva K.V., Nikitina L.P., Gen’ V.S., Kuzmin A.V., Afonin A.V., Trofimov B.A. A straightforward access to 2-hydroxyoxazino[3,2-f]phenanthridines from phenanthridine, oxalylacetylenes and water // Mendeleev Communications. – 2022. – V. 32. – N. 4. – P. 439-442. DOI: 10.1016/j.mencom.2022.07.004
Никитина Л.П., Беляева К.В., Гень В.С., Афонин А.В., Трофимов Б.А. Одновременная N- и C-функционализация акридина этиловыми эфирами арил-2-оксобут-3-иновых кислот в присутствии воды: синтез N-алкенилакридин-9-онов // Доклады Российской академии наук. Химия, науки о материалах. – 2022. – Т. 506. – С. 3-7. DOI: 10.31857/S2686953522600404
3. Неожиданные реакции пирролилацетиленовых кетонов с циклическими иминами
Новые горизонты химического применения ацилпирролилацетиленов открываются в реакции с циклическими иминами. Обнаружено, что они подвергаются легкому [3+2]-циклоприсоединению к 1-пирролинам, 3H-индолам, шести- и семичленным циклическим иминам или 1-метилизохинолину, приводя к ацилметилентетрагидродипирроло[1,2-a:1’,2’-c]имидазолам, -гидропирроло[1’,2’:3,4]имидазо[1,2-a]индолам, -пиридинам, -азепинам или гидропирроло[1’,2’:3,4]имидазо[2,1-a]изохинолинам с выходами до 96% и 90% Е-стереоселективностью.

Oparina L.A., Belyaeva K.V., Kolyvanov N.A., Ushakov I.A., Gotsko M.D., Sobenina L.N., Vashchenko A.V., Trofimov B.A. Catalyst-free annulation of acylethynylpyrroles with 1-pyrrolines: a straightforward access to tetrahydrodipyrrolo[1,2-a:1′,2′-c]imidazoles // Journal of Organic Chemistry. – 2022. – V. 87. – Iss. 15. – P. 9518-9531. DOI: 10.1021/acs.joc.2c00476
Oparina L.A., Kolyvanov N.A., Ushakov I.A., Nikitina L.P., Petrova O.V., Sobenina L.N., Petrushenko K.B., Trofimov B.A. Contributing to biochemistry and optoelectronics: pyrrolo[1’,2’:2,3]imidazo[1,5-a]indoles and cyclohepta[4,5]pyrrolo[1,2-c]pyrrolo[1,2-a]imidazoles via [3+2] annulation of acylethynylcycloalka[b]pyrroles with Δ1-pyrrolines // International Journal of Molecular Science. – 2023. – V. 24. – 3404. https://doi.org/10.3390/ijms24043404
Trofimov B.A., Oparina L.A., Belyaeva K.V., Kolyvanov N.A., Ushakov I.A., Tomilin D.N., Sobenina L.N., Kuzmin A.V. Eco-friendly, in water, catalyst-free assembly of acylethenylpyrroloimidazoindoles from 3H-indoles and acylpyrrolylacetylenes // New Journal of Chemistry. – 2024. – V. 48. – N. 1. – P. 89-95. DOI: 10.1039/d3nj05049a
Oparina L.A., Belyaeva K.V., Kolyvanov N.A., Ushakov I.A., Sagitova E.F., Trofimov B.A. Synthesis of tetrahydropyridino- and deazepano-pyrrolo[1,2-c]imidazolidines via annulation of cyclic imines with acylethynylpyrroles // Synthesis. – 2024. – V. 56. – N. 15. – P. 2347-2360. DOI: 10.1055/a-2282-7827.
Belyaeva K.V., Nikitina L.P., Saliy I.V., Saliy V.S., Afonin A.V., Oparina L.A., Trofimov B.A. Annulation of 1-methylisoquinoline with pyrrolylacetylenic ketones: catalyst-free stereoselective synthesis of (E)-acylethenylpyrrolo[1',2':3,4]imidazo[2,1-a]isoquinolines // Mendeleev communications. – 2024. – V. 34. – N. 5. – P. 691-693. DOI: 10.1016/j.mencom.2024.09.021
Показано, что реакция электронодефицитных ацилпирролилацетиленов с хинолинами, протекающая в среде MeCN, при 80-82 oC, не останавливается на стадии образования [3+2] аннелированных аддуктов. Промежуточные пирроло[1',2':3,4]имидазо[1,2-a]хинолины подвергаются разрыву связи N-Csp2 и приводят к эффективному, стереоселективному синтезу (Е)-2-(2-ацилэтенилпирролил-1)хинолинов, с выходами до 76%. Реакция распространена на фенантридин с образованием (Е)-6-(2-ацилэтенилпирролил-1) фенантридинов (63-66%).

Belyaeva K.V., Nikitina L.P., Oparina L.A., Saliy V.S., Tomilin D.N., Afonin A.V., Trofimov B.A. Catalyst-free nucleophilic substitution of hydrogen in quinoline ring by acylethynylpyrroles: a stereoselective synthesis of 2-(E-2-acylethenylpyrrolyl)quinolines // New Journal of Chemistry. – 2024. – V. 48 – N. 3. – P. 1336-1349. DOI: 10.1039/D3NJ04989B
Показано, что 1-замещенные имидазолы, как ароматические нейтральные нуклеофилы, содержащие циклическую азометиновую связь, катализируют оригинальную [3+3]-циклодимеризацию ацилпирролилацетиленов в бис(ацилметилиден)дипирроло[1,2-a:1',2'-d]пиразины (выходы до 52%), в то время как 1-замещенные бензимидазолы запускают другой каскадный процесс, приводящий к эффективному синтезу 5-(1Н-пиррол-2-ил)-1,6-бензодиазоциноновых ансамблей с выходами до 92%.

Belyaeva K.V., Nikitina L.P., Gen’ V.S., Tomilin I.V., Sobenina L.N., Afonin A.V., Oparina L.A., Trofimov B.A. 1-Methylimidazole as organic catalyst for [3+3]-cyclodimerization of acylethynylpyrroles to bis(acylmethylidene)dipyrrolo[1,2-a:1',2'-d]pyrazines // Catalysts. – 2022. – V. 12. – Iss. 12. – P. 1604 (1-12). DOI: 10.3390/catal12121604
Belyaeva K.V., Nikitina L.P., Gen’ V.S., Saliy I.V., Sobenina L.N., Afonin A.V., Kuzmin A.V., Vashchenko A.V., Trofimov B.A. Benzo[1,4]diazocinone/pyrrole ensembles via the catalyst-free insertion of pyrrolylacetylenic ketones into benzimidazoles // ChemistrySelect. – 2022. – V. 7. – Iss. 45. – P. e202204482 (1-10). DOI: 10.1002/slct.202204482
Belyaeva K.V., Tomilin D.N., Afonin A.V., Trofimov B.A. 5-(1H-Indol-3-yl)-1-methyl-3-phenyl-1,6-benzodiazocin-2(1H)-one // Molbank. – 2022. – V. 2022. – Iss. 4. – P. M1466 (1-3). DOI: 10.3390/M1466
Гранты за последние три года
Грант РНФ № 21-73-10134: " Разработка общей однореакторной и атом-экономной методологии построения пирроло-имидазолидиновых структур на основе новой реакции циклоприсоединения пирролилацетиленов к двойной С=N связи"
Избранные публикации за последние три года
Обзоры
Чарушин В.Н., Вербицкий Е.В., Чупахин О.Н., Воробьева Д.В., Грибанов П.С., Осипов С.Н., Иванов А.В., Мартыновская С.В., Сагитова Е.Ф., Дяченко В.Д., Дяченко И.В., Кривоколыско С.Г., Доценко В.В., Аксенов А.В., Аксенов Д.А., Аксенов Н.А., Ларин А.А., Ферштат Л.Л., Музалевский В.М., Ненайденко В.Г., Гулевская А.В., Пожарский А.Ф., Филатова Е.А., Беляева К.В., Трофимов Б.А., Балова И.А., Данилкина Н.А., Говди А.И., Тихомиров А.С., Щекотихин А.Е., Новиков М.С., Ростовский Н.В., Хлебников А.Ф., Климочкин Ю.Н., Леонова М.В., Ткаченко И.М., Мамедов В.А., Мамедова В.Л., Жукова Н.А., Семёнов В.Э., Синяшин О.Г., Борщев О.В., Лупоносов Ю.Н., Пономаренко С.А., Фисюк А.С., Костюченко А.С., Илькин В.Г., Березкина Т.В., Бакулев В.А., Газизов А.С., Загидуллин А.А., Карасик А.А., Кукушкин М.Е., Белоглазкина Е.К., Голанцов Н.Е., Феста А.А., Воскресенский Л.Г., Мошкин В.С., Буев Е.М., Сосновских В.Я., Миронова И.А., Постников П.С., Жданкин В.В., Юсубов М.С., Ярёменко И.А., Виль В.А., Крылов И.Б., Терентьев А.О., Горбунова Ю.Г., Мартынов А.Г., Цивадзе А.Ю., Стужин П.А., Иванова С.С., Койфман О.И., Буров О.Н., Клецкий М.Е., Курбатов С.В., Яровая О.И., Волчо К.П., Салахутдинов Н.Ф., Панова М.А., Бургарт Я.В., Салоутин В.И., Ситдикова А.Р., Щегравина Е.С., Федоров А.Ю. Успехи в химии гетероциклических соединений в 21 веке // Успехи химии. – 2024. – Т. 93. – N. 7 – RCR5125.
Основные научные статьи
Belyaeva K.V., Nikitina L.P., Gen’ V.S., Tomilin I.V., Sobenina L.N., Afonin A.V., Oparina L.A., Trofimov B.A. 1-Methylimidazole as organic catalyst for [3+3]-cyclodimerization of acylethynylpyrroles to bis(acylmethylidene)dipyrrolo[1,2-a:1',2'-d]pyrazines // Catalysts. – 2022. – V. 12. – N. 12. – Article number 1604. https://doi.org/10.3390/catal12121604
Belyaeva K.V., Nikitina L.P., Gen’ V.S., Saliy I.V., Sobenina L.N., Afonin A.V., Vashchenko A.V., Trofimov B.A. Benzimidazole ring expansion with acylpyrrolylacetylenes: an efficient, catalyst-free, one-pot excess to pyrrolyl-benzodiazocinones // ChemistrySelect. – 2022. – V. 7. – N. 48. – e20220448. DOI: 10.1002/slct.202204482
Oparina L.A., Belyaeva K.V., Kolyvanov N.A., Ushakov I.A., Gotsko M.D., Sobenina L.N., Vashchenko A.V., Trofimov B.A. Catalyst-free annulation of acylethynylpyrroles with 1-pyrrolines: a straightforward access to tetrahydrodipyrrolo[1,2-a:1′,2′-c]imidazoles // J. Org. Chem. – 2022. – V. 87. – N. 15. – P. 9518-9531. DOI: 10.1021/acs.joc.2c00476
Belyaeva K.V., Gen’ V.S., Nikitina L.P., Afonin A.V., Trofimov B.A. Oxalylacetylenes as dielectrophiles for annulation of quinoline ring: synthesis of highly functionalized 1,3-oxazinoquinolines // Synthesis. – 2022. – V. 54. – N. 7. – P. 1833-1842. DOI: 10.1055/a-1644-2930
Oparina L.A., Malkina A.G., Kolyvanov N.A., Ushakov I.A., Saliy I.V., Apartsin K.A., Trofimov B.A. δ-Keto aminoacrylonitriles and δ-keto aminoenones from 1-pyrrolines, cyanoacetylenes, and acetylenic ketones // Synthesis. – 2022. – V. 54. – N. 11. – P. 2635-2646. DOI: 10.1055/a-1742-2736
Oparina L.A., Kolyvanov N.A., Ushakov I.A., Nikitina L.P., Petrova O.V., Sobenina L.N., Petrushenko K.B., Trofimov B.A. Contributing to biochemistry and optoelectronics: pyrrolo[1´,2´:2,3]imidazo[1,5-a]indoles and cyclohepta[4,5]pyrrolo[1,2-c]pyrrolo[1,2-a]imidazoles via [3+2] annulation of acylethynylcycloalka[b]pyrroles with ∆ 1 – pyrrolines // International Journal of Molecular Sciences. – 2023. – V. 24. – N. 4. – P. 3404 (1-16). DOI: 10.3390/ijms24043404
Petrova O.V., Tomilin D.N., Senol H., Belyaeva K.V., Nikitina L.P., Oparina L.A., Sobenina L.N., Trofimov B.A., Sadeghian N., Taslimi P., Farzaliyev V., Sujayev A., Gulçin I. Synthesis of pyrrole-heterocyclic derivatives as anti-Alzheimer and antidiabetic candidates: An in vitro-in silico study // J. Mol. Struct. – 2024. – V. 1315. – 138998. https://doi.org/10.1016/j.molstruc.2024.138998.














