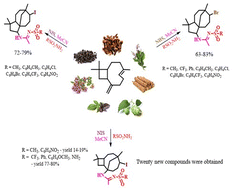
Природный терпен β-кариофиллен, известный своим древесно-пряным ароматом, оказался отличной "заготовкой" для создания новых молекул - причем он кардинально перестраивает свой "скелет". Ученые ФИЦ ИрИХ СО РАН (Институт Фаворского) открыли стерео- и региоселективную реакцию этого соединения с сульфонамидами в присутствии бром- и иодсукцинимида - в результате "собираются" сложные полициклические структуры с отличными выходами.
С N-бромсукцинимидом в продукте всегда формировался декагидроциклопентааннуленовый "скелет" с атомом брома в строго определённом положении, в случае же иода все сложнее - в зависимости от природы сульфонамида, богатство продуктов куда выше. Ученые предложили механизмы этих реакций: сначала происходит галогенирование двойной связи в цикле терпена, затем следует внутримолекулярная циклизация с образованием реакционноспособного карбокатиона. Далее, в зависимости от условий, этот катион либо захватывается молекулой растворителя, либо успевает провести расширение цикла с четырёх- до пятичленного перед тем, как быть перехваченным. Именно эта последовательность и объясняет наблюдаемую высокую стерео- и региоселективность.
Такие работы представляют особый интерес: хотя кариофиллен - редкий гость в растениях Сибири, здесь встречается много других, в том числе и похожих, терпенов. Изучение их химии - важный шаг к созданию новых химических продуктов из возобновляемого сырья.
Результаты исследования опубликованы в международном химическом журнале New Journal of Chemistry
https://pubs.rsc.org/en/content/articlelanding/2026/nj/d5nj03976b