д.х.н., профессор
Потапов Владимир Алексеевич
Заведующий лабораторией
8 (3952) 42-58-85
История лаборатории
Лаборатория халькогенорганических соединений создана на базе группы лаборатории непредельных гетероатомных соединений в январе 1986 года. С 1986 до 2018 года лабораторию возглавляла д.х.н., профессор С.В. Амосова. С 2018 года заведующим лабораторией является д.х.н., профессор В.А. Потапов.
Кадровый состав
В лаборатории халькогенорганических соединений работают 16 человек, 2 доктора наук, 10 кандидатов наук, 2 аспиранта и 2 студента.
Потапов Владимир Алексеевич, д.х.н., проф., зав. лабораторией
Андреев Михаил Викторович, к.х.н., н.с.
Ишигеев Роман Семенович, к.х.н., н.с.
Мартынов Александр Викторович, д.х.н., в.н.с.
Махаева Наталья Александровна, к.х.н., с.н.с.
Мусалов Максим Викторович, к.х.н., в.н.с.
Мусалова Мария Владимировна, к.х.н., с.н.с.
Новокшонова Ирина Анатольевна, к.х.н., н.с.
Филиппов Андрей Сергеевич, к.х.н., н.с.
Хабибулина Альфия Галимулловна, к.х.н., н.с.
Живетьева Светлана Александровна, к.х.н., вед. инж.
Иванова Лилия Алексеевна, инж., аспирант
Корякина Елена Геннадьевна, лаборант
Пакеева Анна Аркадьевна, аспирант
Сороковикова Мария Александровна, вед. инж.
Шкурченко Ирина Владимировна, к.х.н., вед. инж.
Ярошенко Татьяна Исаевна, вед. инж.
Группа химии галогенидов халькогенов и исследования глутатионпероксидаза-подобной активности (руководитель: к.х.н., в.н.с. М.В. Мусалов)
Группа разработки методов функционализации халькогенорганических соединений (руководитель: д.х.н., в.н.с. А.В. Мартынов)
Группа разработки методов синтеза конденсированных халькогеназотсодержащих систем (руководитель: к.х.н., н.с. Р.С. Ишигеев)
Группа химии теллурорганических соединений (руководитель: к.х.н., с.н.с. М.В. Мусалова)
Группа химии сераселенсодержащих гетероциклических соединений (руководитель: к.х.н., с.н.с. Н.А. Махаева)

Потапов Владимир Алексеевич - д.х.н., профессор, заведующий лабораторией. После окончания с отличием ИГУ в 1980 г. поступил в аспирантуру института, которую окончил в 1983 г. с защитой кандидатской диссертации "Реакции селена с ацетиленами - путь к ненасыщенным и функциональным селенорганическим соединениям (научные руководители: академик Б.А. Трофимов и д.х.н., профессор Н.К. Гусарова). В 1993 г. им защищена диссертация на соискание ученой степени доктора химических наук: "Новые методы синтеза селен- и теллурорганических соединений на основе органических дихалькогенидов и элементных халькогенов". В 2000 г. присвоено ученое звание профессора. Под его руководством в лаборатории защищены 11 кандидатских работ, в том числе диссертации 10 аспирантов. Автор более 250 статей и обзоров в центральных отечественных и зарубежных журналах.
Амосова Светлана Викторовна (Тел. 8(3952) 42-58-85. E-mail: amosova@irioch.irk.ru) - д.х.н., профессор, главный научный сотрудник. В 1968 году защитила кандидатскую диссертацию "Реакции некоторых сульфидов и дисульфидов с ацетиленом". В 1979 году защитила докторскую диссертацию "Новые пути синтеза сераорганических мономеров и полупродуктов на основе ацетилена". С 1976 по 1994 год - заместитель директора по науке Иркутского института органической химии СО РАН. В 1983 году получила ученое звание профессора. 15 лет (1986-2001 гг.) Амосова С. В. – заместитель председателя Научного Совета Госкомитета по науке и технике по проблеме «Химия и технология органических соединений серы» и председатель секции этого совета «Синтетическая и теоретическая химия органических соединений серы». Под её руководством защищена 21 кандидатская диссертация. В лаборатории защищены 4 докторских диссертации. В списке ее трудов – монография и семь обзоров, более 400 статей в ведущих отечественных и зарубежных журналах; имеется 250 российских и зарубежных патентов.
Мартынов Александр Викторович (Тел. 8(3952) 42-49-54. E-mail: martynov@irioch.irk.ru.) - д.х.н., ведущий научный сотрудник, руководитель группы. В1980 году защитил кандидатскую диссертацию тему "Исследования реакций тиилирования хлорэтиленов и свойства органил(хлорвинил)сульфидов и сульфонов" (научные руководители: академик М. Г. Воронков и к.х.н. А.Н. Мирскова). В 2007 году защитил докторскую диссертацию "Галогенвинилхалькогениды и бис(органилхалькогено)ацетилены: новые методы синтеза на основеполигалогенэтенов, галогенацетиленов и диэтинилсиланов". В 1993 г. ему присвоено ученое звание старшего научного сотрудника. Автор более 100 статей и обзоров центральных отечественных и зарубежных журналах.
Области исследований / Тематика лаборатории
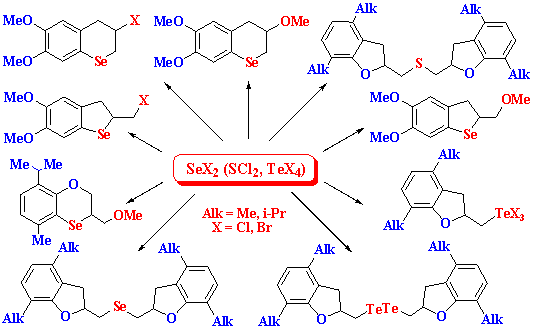
Создание комплекса методов синтеза новых классов и семейств селенорганических соединений на основе уникальных электрофильных реагентов - дихлорида и дибромида селена, впервые введенных в органический синтез в лаборатории халькогенорганических соединений и позволяющих осуществлять широкий ряд хемо-, регио- и стереоселективных реакций, с целью создания новых биологически активных веществ и инновационных материалов.
Развитие эффективной методологии синтеза новых водорастворимых конденсированных производных халькогенсодержащих азотистых гетероциклов на основе реакций аннелирования гетарилхалькогенилгалогенидов с ненасыщенными и природными соединениями с целью получения продуктов с высокой биологической активностью, прежде всего, антимикробной активностью.
Разработка фундаментальных подходов к получению халькогенорганических соединений на основе систематического изучения реакций галогенидов халькогенов (реакций аннелирования, циклизации, присоединения, замещения, аннелирования-функционализации, циклофункционализации) с различными субстратами, в том числе содержащими двойную или тройную связи. Сравнение реакционной способности галогенидов халькогенов (SeCl2, SeBr2, Se2Cl2, Se2Br2, SeCl4, SeBr4, SCl2, S2Cl2, TeCl4, TeBr4) в различных реакциях.
Систематические исследования, направленные на создание новых халькогенорганических продуктов с высокой глутатионпероксидаза-подобной активностью, которые в перспективе могут стать эффективными корректорами вакцинации, препаратами для профилактики и лечения сердечно-сосудистых заболеваний, инсульта головного мозга и инфаркта миокарда. Направленный синтез аналогов и производных известных препаратов (Эбселен, Перхлозон, AS-101, препараты хинолинового и адамантанового ряда и др.) с целью получения новых биологически активных веществ.
Развитие химии дивинилхалькогенидов (дивинилсульфида, дивинилселенида, дивинилтеллурида), их аналогов и производных – уникальных базовых строительных блоков в химии халькогенорганических соединений, полупродуктов и синтонов для органического синтеза.
Изучение химии селенираниевых интермедиатов. Разработка методов синтеза новых классов непредельных сераселенсодержащих соединений с потенциальной биологической активностью на основе производных 1,3-тиаселенола и перегруппировок халькогенсодержащих гетероциклических систем с раскрытием, сужением или расширением цикла.
Создание новых методов гетероциклизации и аннелирования халькогенсодержащих гетероциклических систем на основе использования галогенидов халькогенов с целью получения новых продуктов с высокой глутатионпероксидаза-подобной активностью.
Изучение закономерностей реакций трансфера халькогенов и фундаментального эффекта анхимерного содействия атомов халькогенов.
Разработка комплекса новых регио- и стереоселективных фундаментальных подходов к практически ценным халькогенорганическим соединениям на основе генерирования из элементных халькогенов или органических дихалькогенидов высоко реакционноспособных электрофильных и нуклеофильных реагентов и изучения их реакций с ненасыщенными субстратами и природными соединениями.
Изучение ранее неизвестных реакций тетрагалогенидов теллура с ацетиленами и алкенами с целью разработки стерео- и региоселективных методов синтеза новых функциональных теллурорганических соединений - перспективных полупродуктов для органического синтеза и реагентов для микроэлектроники.

Основные достижения
1.ФУНДАМЕНТАЛЬНЫЙ ПОДХОД К НОВЫМ СЕЛЕН-, ТЕЛЛУР- И СЕРОСОДЕРЖАЩИМ ГЕТЕРОЦИКЛИЧЕСКИМ СОЕДИНЕНИЯМ НА ОСНОВЕ РЕАКЦИЙ АННЕЛИРОВАНИЯ И ЦИКЛОФУНКЦИОНАЛИЗАЦИИ ГАЛОГЕНИДАМИ ХАЛЬКОГЕНОВ ФУНКЦИОНАЛЬНЫХ АЛКЕНОВ И ПРИРОДНЫХ СОЕДИНЕНИЙ (включен в важнейшие достижения РАН: Отчётные материалы Научного совета РАН по органической химии за 2021 год. Российская Академия Наук. Отделение Химии и Наук о Материалах. Москва, 2022. С. 51-52).https://zioc.ru/images/site/otchyotnyie-materialyi-nauchnogo-soveta-ran-po-organicheskoj-ximii-2021.pdf
Разработан фундаментальный подход к новым селен-, теллур- и серосодержащим гетероциклическим соединениям на основе реакций циклофункционализации и аннелирования галогенидами халькогенов функциональных алкенов, природных соединений и их производных (эвгенол, изоэвгенол, метилэвгенол, метилизоэвгенол, ацетилэвгенол, аллиловые и пропаргиловые эфиры тимола, карвакрола и других природных соединений). Новая методология синтеза конденсированных селенсодержащих гетероциклических соединений основана на реакциях аннелирования и аннелирования-алкоксилирования дигалогенидами селена ароматических и природных соединений, содержащих ненасыщенные функции (аллильная, пропенильная, аллилокси-, пропаргилокси- и другие группы). Стадии присоединения, электрофильного ароматического замещения и нуклеофильного замещения реализуются в условиях одной реакции. Важной особенностью методологии является высокая селективность процесса. На основе новой методологии разработан фундаментальный подход к новым ансамблям конденсированных селенсодержащих гетероциклов − функциональным селенохроманам, дигидробензоселенофенам, дигидробензоксаселенинам и другим соединениям.
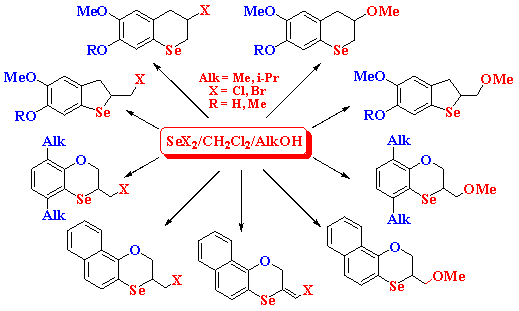
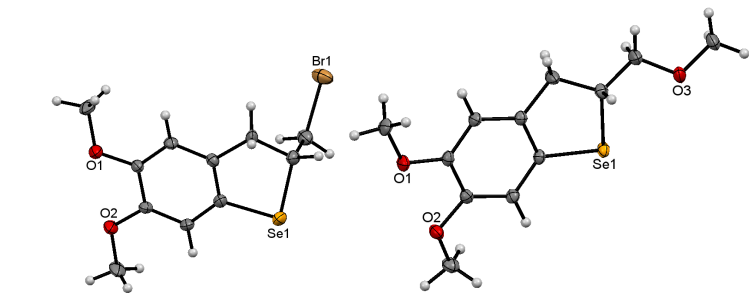
Musalov M.V., Potapov V.A., Yakimov V.A., Musalova M.V., Maylyan A.A., Zinchenko S.V., Amosova S.V. A Regioselective Synthesis of Novel Functionalized Organochalcogen Compounds by Chalcogenocyclofunctionalization Reactions Based on Chalcogen Halides and Natural Products. Molecules. 2021. Vol. 26. Art. ID: 3729. https://doi.org/10.3390/molecules26123729; Musalov M.V., Yakimov V.A., Potapov V.A., Zinchenko S.V., Amosova S.V. One-pot syntheses of functionalized dihydrobenzoselenophenes and selenochromans from acetyl eugenol and selenium dibromide. rearrangement of 2-(bromomethyl)-2,3-dihydro-1-benzoselenophene to selenochromans. Russ. J. Org. Chem. 2021. Vol. 57. P. 558-564. DOI: 10.1134/S1070428021040096; Potapov V.A., Ishigeev R.S., Musalov M.V., Khabibulina A.G., Musalova M.V., Maylyan A.A., Pakeeva A.A., Ivanova L.A., Amosova S.V. Novel heterocyclic and condensed compounds based on annulation and cyclofunctionalization reactions of electrophilic chalcogen reagents. comparison of the reactivity of sulfur, selenium and tellurium halides. 30th Int. Symposium on the Organic Chemistry of Sulfur. Abstracts. Florence, 2024. P. 75.
2. НОВЫЕ КЛАССЫ СЕЛЕНОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С ВЫСОКОЙ ГЛУТАТИОНПЕРОКСИДАЗА-ПОДОБНОЙ АКТИВНОСТЬЮ, КОТОРАЯ ПРЕВЫШАЕТ АКТИВНОСТЬ ПРЕПАРАТА ЭБСЕЛЕН (включено в важнейшие достижения РАН: Отчётные материалы Научного совета РАН по органической химии за 2022 год. Российская Академия Наук. Отделение Химии и Наук о Материалах. Москва, 2023. С. 54-55). https://zioc.ru/images/site/otchyotnyie-materialyi-nauchnogo-soveta-ran-po-organicheskoj-ximii-2022.pdf
На основе элементного селена, пропинамидов и их силильных производных разработаны эффективные регио- и стереоселективные методы синтеза ранее неизвестных классов селенорганических соединений (дивинилселенидов, дивинилдиселенидов и винилорганилселенидов, содержащих амидные функции): (Z)-органил(3-амино-3-оксо-1-пропенил)селенидов, (Z,Z)-бис(3-амино-3-оксо-1-пропенил)селенидов и -диселенидов с высокими выходами. Изучена глутатионпероксидаза-подобная активность полученных продуктов и найдены соединения с высокой активностью, которая превышает активность известного препарата эбселен. Следует отметить, что препарат эбселен с высокой глутатионпероксидаза-подобной и противовоспалительной активностью, который используется за рубежом для лечения и профилактики инсульта и сердечно-сосудистых заболеваний, также содержит амидную группу и атом селена.
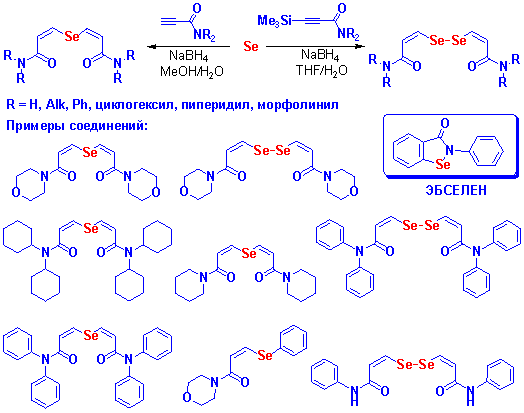
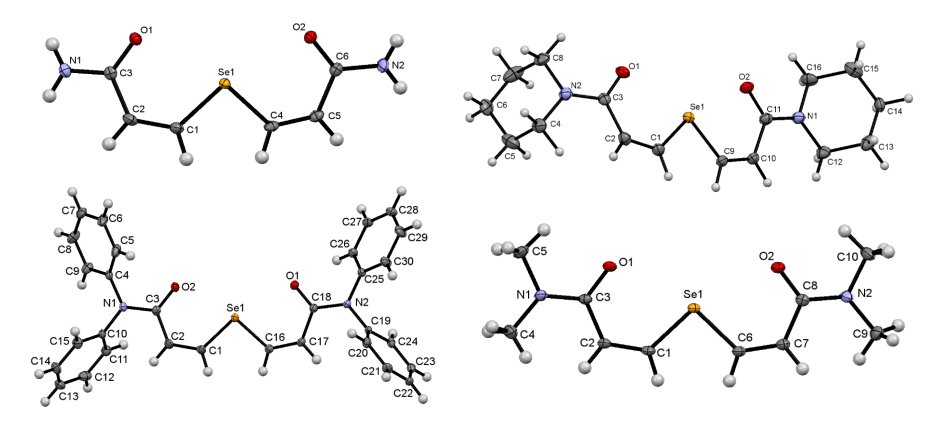
Potapov V.A., Andreev M.V., Musalov M.V., Sterkhova I.V., Amosova S.V., Larina L.I. Regio and stereoselective synthesis of (Z,Z)-bis(3-amino-3-oxo-1-propenyl) selenides and diselenides based on 2-propynamides: a novel family of diselenides with high glutathione peroxidase-like activity. Inorganics. 2022. V. 10. Iss. 6. Art. ID: 74. IF 3,149. DOI: 10.3390/inorganics10060074.
Andreev M.V., Potapov V.A., Musalov M.V., Amosova S.V. (Z,Z)-Selanediylbis(2-propenamides): Novel Class of Organoselenium Compounds with High Glutathione Peroxidase-Like Activity. Regio- and Stereoselective Reaction of Sodium Selenide with 3-Trimethylsilyl-2-propynamides. Molecules. 2020. Vol. 25. Art. ID: 5940. https://doi.org/10.3390/molecules25245940
3. ОТКРЫТИЕ ЯВЛЕНИЯ ТРАНСФЕРА ГАЛОГЕНИДОВ СЕЛЕНА МЕЖДУ МОЛЕКУЛАМИ, ПРОТЕКАЮЩЕГО В РАСТВОРЕ ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ (включено в важнейшие достижения РАН: Отчётные материалы Научного совета РАН по органической химии за 2020 год. Российская Академия Наук. Отделение Химии и Наук о Материалах. Москва, 2021. С. 34-35). https://zioc.ru/images/site/dostigenija-2020-to-print-05032021.pdf
Установлено, что в растворе при комнатной температуре селенорганические соединения могут обмениваться галогенидами селена с ненасыщенными молекулами. Аддукты дибромида селена с алкенами или циклоалкенами легко обмениваются SeBr2 с ненасыщенными соединениями, включая ацетилены, в растворе при комнатной температуре. Аналогичные реакции трансфера с алкена на алкен и с алкена в алкин протекают с аддуктами органилселененилбромидов с алкенами или циклоалкенами. Предполагаемый путь реакции включает генерацию селенираниевых катионов, которые взаимодействуют с новой молекулой алкена или алкина с переносом селенсодержащего реагента. Установлено, что эффективными реагентами для осуществления реакций трансфера являются Se(CH2CH2Br)2 и RSeCH2CH2Br. На основе реакций трансфера разработаны регио- и стереоселективные методы синтеза ранее неизвестных органил-E-2-бромвинилселенидов, бис(E-2-бромовинил)селенидов и других ценных селенорганических соединений с количественными выходами.
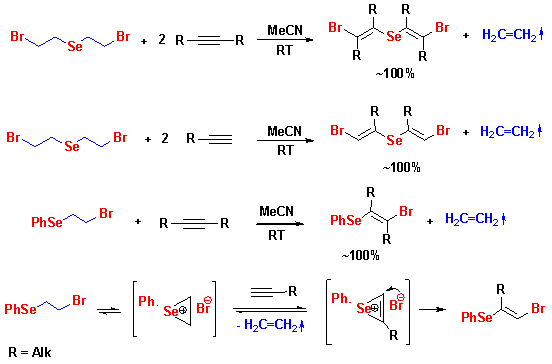
Potapov V.A., Musalov M.V., Kurkutov E.O., Yakimov V.A., Khabibulina A.G., Musalova M.V., Amosova S.V., Borodina T.N., Albanov A.I. Remarkable Alkene-to-Alkene and Alkene-to-Alkyne Transfer Reactions of Selenium Dibromide and PhSeBr. Stereoselective Addition of Selenium Dihalides to Cycloalkenes. Molecules. 2020. Vol. 25, Art. ID: 194. DOI: 10.3390/molecules25010194
4. КОМПЛЕКС ЭФФЕКТИВНЫХ МЕТОДОВ ТРАНСАННУЛЯРНОЙ БИС-ФУНКЦИОНАЛИЗАЦИИ ЦИКЛООКТАДИЕНА ДИГАЛОГЕНИДАМИ СЕЛЕНА ДЛЯ ПОЛУЧЕНИЯ НОВЫХ СЕЛЕНОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С ВЫСОКОЙ ГЛУТАТИОНПЕРОКСИДАЗА-ПОДОБНОЙ АКТИВНОСТЬЮ (включено в важнейшие достижения РАН: Отчётные материалы Научного совета РАН по органической химии за 2023 год. Российская Академия Наук. Отделение Химии и Наук о Материалах. Москва, 2024. С. 54-55). https://zioc.ru/images/site/book-2023-to-print.pdf
На основе реакций дибромида селена с циклооктадиеном в присутствии нуклеофильных реагентов разработан комплекс эффективных методов трансаннулярной бис-функционализации с целью синтеза новых функционализированных соединений. В ряду синтезированных продуктов открыты селенорганические соединения, проявляющие высокую глутатионпероксидаза-подобную активность и значительно повышающие активность глутатионредуктазы. Такое сочетание активности не описано в литературе. Наиболее активными являются водорастворимые 2,6-бис(2-гидроксиэтилокси)- и 2,6-дигидрокси-9-селенабицикло[3.3.1]нонаны. Полученные продукты в перспективе могут стать препаратами для профилактики и лечения сердечно-сосудистых заболеваний, инсульта головного мозга и инфаркта миокарда.
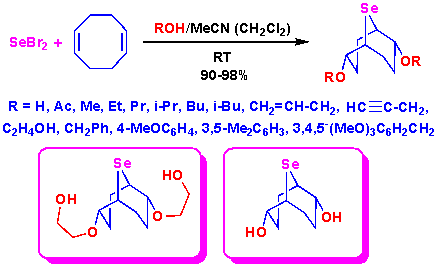
Musalov M.V., Kapustina I.S., Spiridonova E.V., Ozolina N.V., Amosova S.V., Borodina T.N., Potapov V.A. Transannular Selenocyclofunctionalization of 1,5-cyclooctadiene: The Antioxidant Properties of 9-selenabicyclo[3.3.1]nonane Derivatives and the Discovery of Increasing Both GPx and GR Activities. Inorganics. 2023. Vol. 11. Art. ID: 304 (1-15). https://doi.org/10.3390/inorganics11070304
5. РАЗРАБОТКА КОМПЛЕКСА МЕТОДОВ СИНТЕЗА НОВЫХ КЛАССОВ И СЕМЕЙСТВ ФУНКЦИОНАЛЬНЫХ И ГЕТЕРОЦИКЛИЧЕСКИХ СЕЛЕНОРГАНИЧЕСКИХ СОЕДИНЕНИЙ НА ОСНОВЕ РЕАКЦИЙ ДИХЛОРИДА И ДИБРОМИДА СЕЛЕНА
Ранее в лаборатории халькогенорганических соединений впервые введены в органический синтез дихлорид и дибромид селена. Эти электрофильные реагенты не могут быть выделены в чистом виде и в растворе быстро подвергаются диспропорционированию. Для эффективного использования этих реагентов разработана новая методология, которая позволила вовлекать их в разнообразные реакции с целью получения новых классов и семейств селенорганических соединений. Дихлорид и дибромид селена получают in situ действием на элементный селен галогенирующих реагентов и немедленно вовлекают в последующие реакции. Впервые разработан метод генерации дибромида селена из элементного селена и брома.
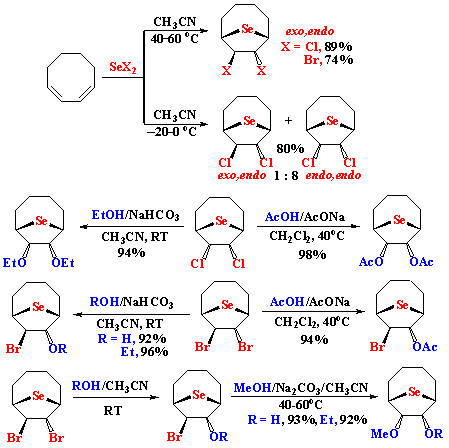
Впервые осуществлена реакция трансаннулярного присоединения дихлорида и дибромида селена к 1,3-циклоктадиену, на основе которой разработаны регио- и стереоселективные подходы к новым 2,3-бифункциональным производным 9-селенабицикло[4.2.1]нонана с эндо-экзо и эндо-эндо стереоконфигурациями. Найдены условия для реакций стереоселективного трансаннулярного анти,син- и анти,анти-присоединения. Разработан метод последовательного введения двух различных функциональных групп в структуру 9-селенабицикло[4.2.1]нонана, который основан на разной реакционной способности галогенов в син- и анти-положении по отношению к атому селена. В случае анти-положения по отношению к атому селена, атом галогена значительно активирован к нуклеофильному замещению за счет высокого анхимерного эффекта атома селена (Accurso A.A., Cho S.-H., Amin A., Potapov V.A., Amosova S.V., Finn M.G. Thia-, Aza-, and Selena[3.3.1]bicyclononane Dichlorides: Rates vs Internal Nucleophile in Anchimeric Assistance. J. Org. Chem. 2011. Vol. 76. P. 4392. https://doi.org/10.1021/jo102440k). Это открывает возможности последовательного введения двух разных функциональных групп в молекулу 9-селенабицикло[4.2.1]нонана в различных условиях.
Musalov M.V., Pakeeva A.A., Potapov V.A. Synthesis of New Derivatives of 9-Selenabicyclo[4.2.1]nonane by the Transannular Addition of Selenium Dihalides to 1,3-Cyclooctadiene. Russian Journal of Organic Chemistry. 2025. Vol. 61. No. 11. P. 2097-2103. DOI: 10.1134/S1070428025604789
6. НОВЫЕ РЕАГЕНТЫ В ОРГАНИЧЕСКОМ СИНТЕЗЕ: ХИНОЛИН-2-СУЛЬФЕНИЛГАЛОГЕНИДЫ. СИНТЕЗ НОВЫХ ПРОИЗВОДНЫХ [1,3]ТИАЗОЛО[3,2-а]ХИНОЛИНИЯ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ
Впервые показана возможность генерации из хинолин-2-тиола новых реагентов: хинолин-2-сульфенилхлорида и -бромида, которые введены в органический синтез на примере реакций аннелирования с алкенами и природными соединениями. На этой основе разработан селективный метод синтеза новых производных [1,3]тиазало[3,2-a]хинолиния с высокими выходами. В результате исследования антимикробных свойств полученных продуктов найдены соединения с высокой антибактериальной активностью.
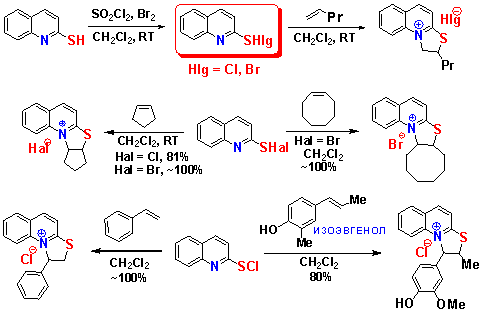
Potapov V.A., Ishigeev R.S., Amosova S.V. Efficient regioselective synthesis of novel condensed sulfur-nitrogen heterocyclic compounds based on annulation reactions of 2-quinolinesulfenyl halides with alkenes and cycloalkenes. Molecules. 2021. V. 26. Iss. 16. Art. ID: 4844 (1-16). IF 4,411. DOI: 10.3390/molecules26164844
7. НОВОЕ СЕЛЕНОРГАНИЧЕСКОЕ СОЕДИНЕНИЕ С ВЫСОКОЙ ГЛУТАТИОНПЕРОКСИДАЗА-ПОДОБНОЙ АКТИВНОСТЬЮ КАК ЭФФЕКТИВНЫЙ КОРРЕКТОР ВАКЦИНАЦИИ С ИММУНОГЕННЫМИ И ПРОТЕКТИВНЫМИ СВОЙСТВАМИ
Создание новых препаратов с глутатионпероксидаза-подобной активностью даст возможность уменьшить распространение таких социально значимых заболеваний, как инсульт головного мозга, инфаркт миокарда, сердечно-сосудистые и раковые заболевания, диабет, артрит, болезни Альцгеймера и Паркинсона. В основе развития многих из данных заболеваний лежат процессы нарушения антиоксидантно-антирадикальной защиты организма и перекисного окисления липидов. В ведущих странах мира интенсивно ведутся поиски селенорганических соединений с высоким глутатионпероксидаза-подобным эффектом, которые являются катализаторами нейтрализации перекисных и радикальных соединений в организме человека, а селенсодержащий препарат эбселен используется за рубежом для лечения и профилактики инсульта и инфаркта.
Разработан эффективный метод синтеза дибромида 2,6-дипиридиний-9-селенабицикло[3.3.1]нонана и его производных на базе дигалогенидов селена, циклооктадиена и функциональных пиридинов. Установлено, что дибромид 2,6-дипиридиний-9-селенабицикло[3.3.1]нонана обладает высокой глутатионпероксидаза-подобной активностью и является эффективным корректором вакцинации с иммуногенной и протективной активностью (совместно с Противочумным институтом Сибири и Дальнего востока получен патент RU 2815337).
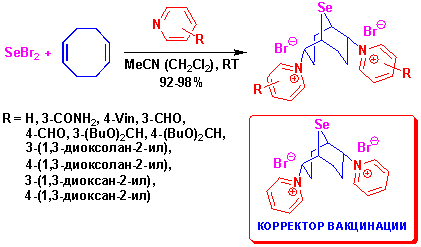
Дубровина В.И., Юрьева О.В., Пятидесятникова А.Б., Старовойтова Т.П., Потапов В.А., Мусалов М.В., Иванова Т.А., Балахонов С.В. Патент на изобретение RU 2815337 C1, 13.03.2024. Бюллетень. 2024. № 8. Пятидесятникова А.Б., Дубровина В.И., Юрьева О.В., Корытов К.М., Иванова Т.А., Потапов В.А., Мусалов М.В., Балахонов С.В. Влияние селенорганического соединения 974zh на экспрессию генов TLR2 и TLR4 в клетках крови и селезёнки экспериментальных животных при совместном введении с Yersinia pestis EV // Acta biomedica scientifica. 2024. Т. 9. N 3. С. 249-255. DOI: 10.29413/ABS.2024-9.3.25. Musalov M.V., Zhivet’eva S.A., Shkurchenko I.V., Amosova S.V., Potapov V.A. Synthesis of 2,6-dibromo-9-selenabicyclo[3.3.1]nonane-based pyridinium salts containing acetal groups. Russ. J. Org. Chem. 2022. Vol. 58. P. 628-632. DOI: 10.1134/S1070428022040236
8. КОМПЛЕКС СЕЛЕКТИВНЫХ МЕТОДОВ СИНТЕЗА 2- И 3-ФУНКЦИОНАЛЬНЫХ ВОДОРАСТВОРИМЫХ ПРОИЗВОДНЫХ [1,3]СЕЛЕНАЗОЛО[3,2-а]- И -[1,3]ТИАЗОЛО[3,2-а]ПИРИДИНИЯ С ВЫСОКОЙ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ
На основе систематических исследований реакций аннелирования 2-пиридинселененил- и 2-пиридинсульфенилгалогенидов с ненасыщенными природными (эвгенол, изоэвгенол, инден, анетол и их производные), гетероциклическими и винилгетероатомными соединениями (виниловые эфиры, винилсульфиды, винилселениды, виниламиды) разработаны селективные методы синтеза новых семейств конденсированных водорастворимых производных [1,3]селеназоло[3,2-а]пиридиния и [1,3]тиазоло[3,2-а]пиридиния с высокими и количественными выходами. Впервые введен в органический синтез 2-пиридинсульфенилиодид, что позволило осуществить ряд ранее неизвестных реакций. На схеме представлены два пути региоселективных реакций, протекающих либо через промежуточные карбокатионы С, которые стабилизируются соседним гетероатомом, либо через тиираниевые или селенираниевые интермедиаты D с селективным образованием соответственно 3- или 2-функциональных производных.
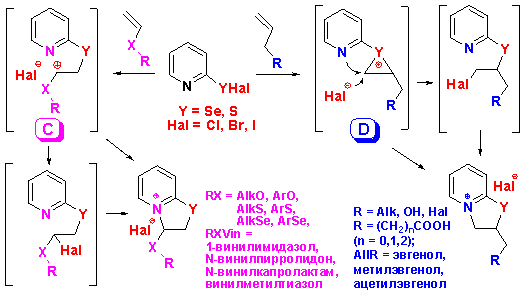
На основе исследования антибактериальных свойств полученных продуктов против грамположительных и грамотрицательных бактерий найдены соединения с высокой активностью. При сравнении активности аналогичных сера- и селенсодержащих продуктов установлено, что селенсодержащие соединения проявляют более высокую активность, чем их сернистые аналоги.
Potapov V.A., Ishigeev R.S., Belovezhets L.A., Amosova S.V. Novel Family of Selenazolo[3,2-a]pyridinium Derivatives Based on Annulation Reactions and Comparative Analysis of Antimicrobial Activity of the Selenium and Sulfur Analogs of Chalcogenazolo[3,2-a]pyridiniums. Curr. Org. Chem. 2025. Vol. 29. P. 669-678. DOI: 10.2174/0113852728326804240828071148
9. НОВАЯ ХИМИЯ СЕЛЕНИРАНИЕВЫХ ИНТЕРМЕДИАТОВ НА ОСНОВЕ РЕАКЦИЙ НУКЛЕОФИЛОВ ПО ТРЕМ ЦЕНТРАМ СЕЛЕНИРАНИЕВОГО КАТИОНА С ОБРАЗОВАНИЕМ НОВЫХ ПРОИЗВОДНЫХ 1,4-ТИАСЕЛЕНИНА, 1,3-ТИАСЕЛЕНОЛА И ЛИНЕЙНЫХ НЕНАСЫЩЕННЫХ СОЕДИНЕНИЙ
Под руководством д.х.н., профессора С.В. Амосовой разработан комплекс методов синтеза новых семейств ненасыщенных сераселенсодержащих соединений, протекающих через генерацию селенираниевого интермедиата. В зависимости от природы нуклеофила и условий реакции, нуклеофильная атака может идти по трем разным центрам селенираниевого катиона, приводя к разнообразным сераселенсодержащим продуктам: производным 1,4-тиаселенина, 1,3-тиаселенола или линейным ненасыщенным соединениям.
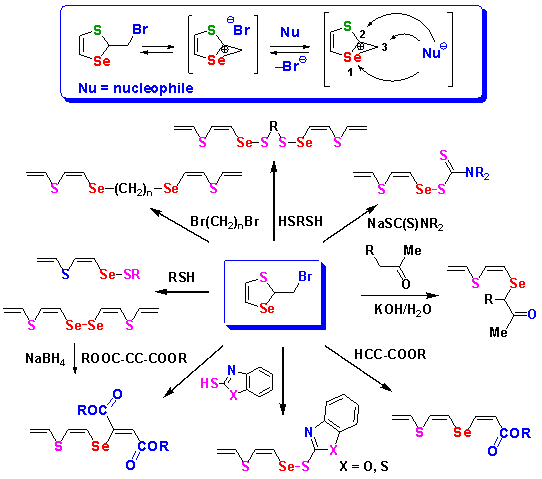
Amosova S.V., Filippov A.S., Makhaeva N.A., Albanov A.I., Potapov V.A. Polyunsaturated sulfur/selenium containing products based on regio- and stereoselective nucleophilic addition and substitution reactions of 1,2-bis[(Z)-2-(vinylsulfanyl)ethenyl] diselane. New J. Chem. 2023. Vol. 47. P. 11505-11514. https://doi.org/10.1039/D3NJ01147J
Amosova S.V., Filippov A.S., Makhaeva N.A., Albanov A.I., Potapov V.A. Regio- and stereoselective synthesis of new ensembles of diversely functionalized 1,3-thiaselenol-2-ylmethyl selenides by a double rearrangement reaction. Beilstein J. Org. Chem. 2020. Vol. 16. P. 515-523. https://doi.org/10.376
10. КОМПЛЕКС МЕТОДОВ СИНТЕЗА НОВЫХ ПРОИЗВОДНЫХ 1,4-ТИАСЕЛЕНИНА И 1,3-ТИАСЕЛЕНОЛА, ПРОТЕКАЮЩИХ ЧЕРЕЗ ГЕНЕРАЦИЮ СЕЛЕНИРАНИЕВОГО ИНТЕРМЕДИАТА И СОПРОВОЖДАЮЩИХСЯ ПЕРЕГРУППИРОВКАМИ
Реакция 2-бромметил-1,3-тиаселенола с селеноцианатом калия при низкой температуре протекает через селенираниевый интермедиат и сопровождается перегруппировкой с расширением цикла и образованием 1,4-тиаселенин-2-илселеноцианата (соединение А). На основе генерации при охлаждении из соединения А 1,4-тиаселенин-2-илселенолат-аниона и вовлечение в реакции нуклеофильного замещения и присоединения с различными субстратами в условиях межфазного катализа (PTC, Phase Transfer Catalysis) разработан комплекс методов синтеза новых производных 1,4-тиаселенина.
Тиаселенин-2-илселеноцианат А используется in situ без выделения. При нагревании 1,4-тиаселенин-2-илселеноцианата А до комнатной температуре протекает перегруппировка через селенираниевый интермедиат с сужением цикла и образованием 1,3-тиаселенол-2-илселеноцианата (соединение В). На основе генерации из соединения В 1,3-тиаселенол-2-илселенолат-аниона с последующими реакциями с различными субстратами в условиях межфазного катализа разработан комплекс методов синтеза новых производных 1,3-тиаселенола.
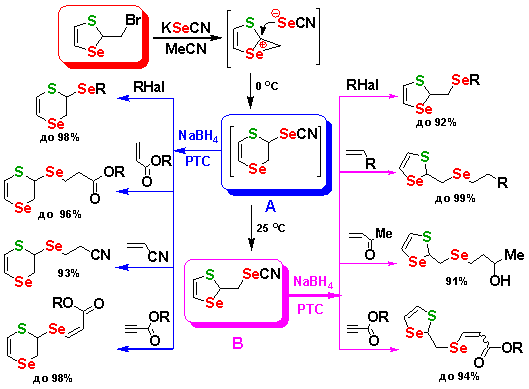
Amosova S.V., Filippov A.S., Potapov V.A. Albanov A.I. Regio- and stereoselective one-pot synthesis of new heterocyclic compounds with two selenium atoms based on 2-bromomethyl-1,3-thiaselenole using phase transfer catalysis. Catalysts. 2022. Vol. 12. Art. ID: 1236. https://doi.org/10.3390/catal12101236
Filippov A.S., Amosova S.V., Makhaeva N.A., Albanov A.I., Potapov V.A. Efficient regioselective synthesis of novel ensembles of organylselanyl-functionalized divinyl sulfides and 1,3-thiaselenoles under phase transfer catalysis conditions, Catalysts. 2023. Vol. 13. Art. ID: 1227. https://doi.org/10.3390/catal13081227
11. РЕГИОСЕЛЕКТИВНЫЙ МЕТОД СИНТЕЗА НОВЫХ ПРОИЗВОДНЫХ [1,4]ТИАЗИНО[2,3,4-IJ]ХИНОЛИНИЯ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ НА ОСНОВЕ РЕАКЦИЙ АННЕЛИРОВАНИЯ ХИНОЛИН-8-СУЛЬФЕНИЛХЛОРИДА И -БРОМИДА
Показана возможность генерации хинолин-8-сульфенилбромида, который впервые введен в органический синтез на примере реакций аннелирования с алкенами. На основе реакций аннелирования хинолин-8-сульфенилхлорида и -бромида с различными ненасыщенными функциональными и гетероциклическими соединениями (алкены, виниловые эфиры, алкилвинилсульфиды, алкилвинилселениды, тетравинилсилан, дивинилсульфид, дивинилселенид и др.) разработаны высоко эффективные региоселективные методы синтеза новых водорастворимых производных [1,4]тиазино[2,3,4-ij]хинолиния.
Присоединение атома серы в реакциях аннелирования с виниловые эфирами, N-винилгетероциклическими соединениями, алкилвинилсульфидами, алкилвинилселенидами, дивинилсульфидом и дивинилселенидом идет по терминальному атому углерода двойной связи по правилу Марковникова. При использовании 1-алкенов, аллилгалогенидов, аллиловых эфиров и сульфидов присоединение атома серы в реакциях аннелирования протекает против правила Марковникова через образование селенираниевого интермедиата. В случае винилсиланов важную роль для регионаправленности против правила Марковникова играет известный бета-эффект атома кремния.
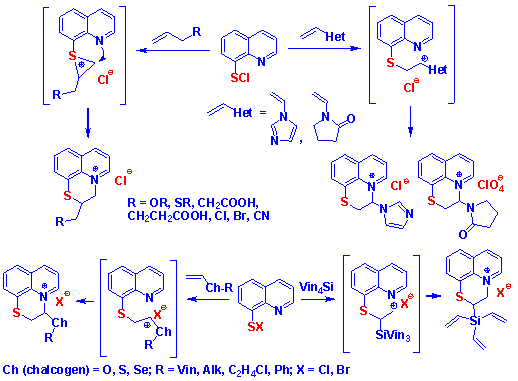
В результате исследования антимикробных свойств полученных продуктов найдены соединения с высокой антибактериальной активностью.
Potapov V.A., Ishigeev R.S., Belovezhets L.A., Amosova S.V. A novel family of [1,4]thiazino[2,3,4-ij]quinolin-4-ium derivatives: regioselective synthesis based on unsaturated heteroatom and heterocyclic compounds and antibacterial activity. Molecules. 2021. V. 26. Iss. 18. Art. ID: 5579 (1-15). IF 4,411. DOI: 10.3390/molecules26185579
Potapov V.A., Ishigeev R.S., Amosova S.V. Efficient regioselective synthesis of novel water-soluble 2H,3H-[1,4]thiazino[2,3,4-ij]quinolin-4-ium derivatives by annulation reactions of 8-quinolinesulfenyl halides. Molecules. 2021. V. 26. Iss. 4. Art. ID: 1116 (1-12). IF 4,411. DOI: 10.3390/molecules26041116
Премия МАИК
Присуждена премия МАИК "Наука-интерпериодика" авторскому коллективу С.В. Амосовой, В.А. Потапову, А.В. Мартынову, М.В. Мусалову, М.В. Пензику, М.В. Мусаловой, Н.А. Махаевой, А.Г. Хабибулиной за лучший цикл работ в "Журнале органической химии" в 2012 г. "Разработка эффективных регио- и стереоселективных способов получения новых халькогенорганических соединений на основе реакций галогенидов халькогенов, в том числе новых электрофильных реагентов дигалогенидов селена, впервые введенных в органический синтез".

Авторский коллектив цикла работ
Диссертации на соискание ученой степени доктора химических наук
Потапов В.А. "Новые методы синтеза селен- и теллурорганических соединений на основе органических дихалькогенидов и элементных халькогенов" (Иркутск, 1993).
Мусорин Г.К. "Новые возможности диметилсульфоксида в синтезе халькогенорганических соединений" (Иркутск, 1996).
Мартынов А.В. "Галогенвинилхалькогениды и бис(органилхалькогено)ацетилены: новые методы синтеза на основе полигалогенэтенов, галогенацетиленов и диэтинилсиланов" (Иркутск, 2007).
Диссертации на соискание ученой степени кандидата химических наук
Белозерова О.В. "Новые способы получения халькогенорганических соединений на основе реакций присоединения халькогенсодержащих реагентов к ацетилену и его производным" (Иркутск, 2006).
Махаева Н.А. «Синтез функциональных органических халькогенидов, содержащих азот, фосфор, кремний, германий» (Иркутск, 2007).
Пензик М.В. Синтез новых селенсодержащих гетероциклов на основе реакций присоединения ди- и тетрагалогенидов селена к дивинилхалькогенидам и замещенным диэтинилсиланам и -германам (Иркутск, 2009).
Куркутов Е.О. “Реакции дихлорида и дибромида селена с алкенами и их кислоро- и серусодержащими производными" (Иркутск, 2010).
Хуриганова О.И. “ Реакции дихлорида и дибромида селена с алкинами и аренами " (Иркутск, 2010).
Мусалов М.В. “Реакции галогенидов селена с ацетиленом, его производными и диаллилхалькогенидами" (Иркутск, 2011).
Мусалова М.В. “Синтез новых ненасыщенных теллурорганических соединений на базе теллура, ацетилена и его производных " (Иркутск, 2012).
Малинович Д.А. "Синтез ненасыщенных халькогенорганических производных азотсодержащих гетероциклов и реакции их аннелирования" (Иркутск, 2013).
Ишигеев Р.С. "Синтез новых гетероциклических соединений на основе ди(2-пиридинил)- и ди(8-хинолинил)дихалькогенидов, дигалогенидов халькогенов и алкенов" (Иркутск, 2020).
Филиппов А.С."Региоселективные методы синтеза новых ненасыщенных серо- и селенсодержащих соединений на основе реакций 2-бромметил-1,3-тиаселенола с халькоген-центрированными нуклеофилами" (Иркутск, 2021).
Якимов В.А."Синтез новых селенсодержащих конденсированных гетероциклических соединений на основе дигалогенидов селена" (Иркутск, 2022).
Гранты РНФ и РФФИ
Грант РФФИ № 14-03-92705 (Российско-Индийский) "Новые конденсированные гетероциклические системы с различным положением в кольцах гетероатомов азота и халькогенов на основе азотсодержащих гетероциклов, содержащих винил-, аллил- и пропаргилхалькогеногруппы" (руководитель: д.х.н., профессор Потапов В.А.).
Грант РНФ № 14-13-01085 "Разработка фундаментального подхода к новым аннелированным и функциональным халькогенорганическим соединениям и биологически активным препаратам на основе галогенидов халькогенов" (руководитель: д.х.н., профессор Потапов В.А.).
Грант РФФИ № 14-03-00185_а "Новые теллурэлементсодержащие органические гетероциклы на основе аддуктов электрофильных реакций тетрагалогенидов теллура с пропаргилгалогенидами" (Руководитель: д.х.н. Мартынов А.В.).
Грант РФФИ № 14-03-31939_мол_а: "Разработка методов синтеза новых классов непредельных сераселенсодержащих функционализированных соединений на основе новых регио- и стереоселективных реакций и перегруппировок 2-бромметил-1,3-тиаселенола" (Руководитель: к.х.н. Пензик М.В.).
Грант РФФИ № 14-03-31910_мол_а: "Кросс-сочетание ацетилена и его производных: разработка фундаментального подхода к получению практически ценных ненасыщенных соединений, их реакции с дигалогенидами селена, селенидами и органилселенолатами щелочных металлов" (Руководитель: к.х.н. М.В. Мусалов).
Грант РФФИ № 14-03-31911_мол_а: "Разработка регио- и стереоспецифических способов получения новых теллурорганических соединений, содержащих Z- и E-2-галогенвинильные группы, и их использование в стереоселективном синтезе алкенов" (Руководитель: к.х.н. М.В. Мусалова).
Грант РФФИ № 16-03-00591 "Разработка нового фундаментального подхода к новым классам непредельных функционализированных сераселенорганических соединений и гетероциклов с потенциальной биологической активностью на основе генерирования селенираниевого интермедиата из 2-бромметил-1,3-тиаселенола" (руководитель: д.х.н., профессор Амосова С.В.)
Грант РФФИ № 16-33-60199_мол_а_дк «Разработка регио- и стереоселективных методов синтеза практически важных функциональных и гетероциклических теллурорганических соединений на основе тетрагалогенидов теллура и их использование в органическом синтезе» (руководитель: к.х.н. Мусалова М.В.)
Грант РФФИ № 18-03-00859 "Разработка эффективных однореакторных методов синтеза новых селенсодержащих конденсированных гетероциклических систем и их функционализации на основе анхимерного эффекта атома селена" (руководитель: к.х.н. Мусалов М.В.)
Грант РФФИ №18-03-01007 "Новые региоспецифичные реакции халькогенофункционализации - путь к ранее неизвестным гетероциклическим и функциональным халькогенорганическим соединениям и исследование их глутатионпероксидаза-подобной активности" (руководитель: д.х.н., профессор Потапов В.А.)
Грант РНФ №18-13-00372 "Разработка на базе элементных халькогенов фундаментальных подходов к новым классам гетероциклических и функционализированных халькогенорганических соединений и изучение их биологической активности с целью обнаружения веществ, перспективных для создания лекарственных препаратов" (руководитель: д.х.н., профессор Потапов В.А.)
Грант РФФИ №19-33-90214 Аспиранты "Разработка эффективных однореакторных методов синтеза новых селенсодержащих конденсированных гетероциклических систем и их функциональных производных на основе дигалогенидов селена (руководитель: к.х.н. М.В.Мусалов)
Грант РФФИ №20-43-383002 р_мол_а "Разработка эффективных общих стратегий синтеза и функционализации халькогенополицикланов и изучение их биологической активности in vivo" (руководитель: к.х.н. М.В.Мусалов).
Грант РНФ №22-13-00339 " Комплекс фундаментальных синтетических подходов к новым семействам гетероциклических соединений, аналогам и производным противовирусных и антибактериальных (фторхинолоновых) препаратов и исследование их биологической активности с целью создания новых лекарственных средств" (руководитель: д.х.н., профессор Потапов В.А.).
Патенты
Дубровина В.И., Юрьева О.В., Пятидесятникова А.Б., Старовойтова Т.П., Потапов В.А., Мусалов М.В., Иванова Т.А., Балахонов С.В. Способ повышения иммуногенной и протективной активности вакцинного штамма чумного микроба.Патент на изобретение RU 2815337. Бюллетень. 2024. № 8.
Трофимов Б.А., Амосова С.В., Елохина В.Н., Ярошенко Т.И., Потапов В.А. Способ получения фармакопейного перхлората 4-тиоуреидоиминометилпиридиния, обладающего высокой туберкулостатической активностью. Патент на изобретение RU 2476426. Бюллетень. 2013. № 6. (Препарат включен в перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения в Российской Федерации).
Обзоры в зарубежных журналах (2022-2026)
MakhaevaN.A., Amosova S.V., Potapov V.A. Recent advances in design and synthesis of diselenafulvenes, tetraselenafulvalenes, and their tellurium analogs and application for materials sciences // Molecules. – 2022. – V. 27. – Iss. 17. – Art. ID: 5613 (1-33). IF 4,927. DOI: 10.3390/molecules27175613
MusalovM.V., Potapov V.A., Musalova M.V., Amosova S.V., Krivdin L.B. Recent developments in the synthesis of organoselenium compounds based on the reactions of organic diselenides with acetylenes // Catalysts. – 2023. – V. 13. – Iss. 10. – Art. ID: 1369 (1-29). IF 3,9. DOI: 10.3390/catal13101369
Martynov A.V. Elemental selenium in the synthesis of selenaheterocycles // Inorganics. – 2023. – V.11. – Iss. 7. – ID:287 (1-37). IF 2,9. DOI: 10.3390/inorganics11070287
Amosova S.V., Makhaeva N.A. Recent advances in design and synthesis of 1,3-thiaselenolane and 1,3-thiaselenole derivatives // Catalysts. – 2023. – V. 13. – Iss. 8. – ID:1221 (1-20). IF 3,9. DOI: 10.3390/catal13081221
Ishigeev R.S., Potapov V.А. Pyridine-2-selanyl chloride in the synthesis of condensed heterocycles // Chemistry of Heterocyclic Compounds. – 2024. – V. 60. – N 9/10. – P. 436-438. DOI: 10.1007/s10593-024-03359-3 IF: 1,3 Q3 БС: 3
Martynov A.V. Elemental tellurium in organoelement synthesis of tellurium-containing organometallics and telluracycles. Journal of Organometallic Chemistry. 2024. V. 1022. ID:123418 (1-35). DOI: 10.1016/j.jorganchem.2024.123418
Makhaeva N.A., Amosova S.V., Filippov A.S., Potapov V.A., Musalov M.V. Recent advances in design, synthesis, and biological activity studies of 1,3-selenazoles // Biomolecules. – 2024. – V. 14. – Iss. 12. – ID: 1546 (1-45). DOI: 10.3390/biom14121546 IF: 4,8.
Martynov A.V. Recent advances in synthesis of telluracycles. Journal of Organometallic Chemistry, 2026, Vol. 1049. Art. ID: 124061. https://doi.org/10.1016/j.jorganchem.2026.124061
Статьи в зарубежных журналах за 5 лет (2021-2025)
PotapovV.A., Ishigeev R.S., Amosova S.V. Efficient regioselective synthesis of novel water-soluble 2H,3H-[1,4]thiazino[2,3,4-ij]quinolin-4-ium derivatives by annulation reactions of 8-quinolinesulfenyl halides // Molecules. – 2021. – V. 26. – Iss. 4. – Art. ID: 1116 (1-12). IF 4,412. DOI: 10.3390/molecules26041116
PotapovV.A., Ishigeev R.S., Belovezhets L.A., Shkurchenko I.V., Amosova S.V. New water-soluble condensed heterocyclic compounds with antimicrobial activity based on annulation reactions of 8-quinolinesulfenyl halides with natural products and alkenes // Applied Sciences-Basel. – 2021. – V. – Iss. 18. – Art. ID: 8532 (1-15). IF 2,679. DOI: 10.3390/app11188532
Ishigeev R.S., Potapov V.A., Shkurchenko I.V., Khabibulina A.G., Amosova S.V. Synthesis of new polycyclic compounds via the reaction of quinoline-8-sulfenyl halides with cyclic alkenes // Chemistry of Heterocyclic Compounds. – 2021. – V. 57. – Iss. 3. – P. 314-319. IF 1,277. DOI: 10.1007/s10593-021-02909-3
Potapov V.A., Ishigeev R.S., Amosova S.V. Efficient regioselective synthesis of novel condensed sulfur-nitrogen heterocyclic compounds based on annulation reactions of 2-quinolinesulfenyl halides with alkenes and cycloalkenes // Molecules. – 2021. – V. 26. – Iss. 16. – ID:4844 (1-16). IF 4,412. DOI: 10.3390/molecules26164844
Potapov V.A., Ishigeev R.S., Belovezhets L.A., Amosova S.V. A novel family of [1,4]thiazino[2,3,4-ij]quinolin-4-ium derivatives: regioselective synthesis based on unsaturated heteroatom and heterocyclic compounds and antibacterial activity // Molecules. – 2021. – V. 26. – Iss. 18. – ID:5579 (1-15). IF 4,412. DOI: 10.3390/molecules26185579
Musalov M.V., Potapov V.A., Amosova S.V. Efficient synthesis of a new family of 2,6-disulfanyl-9-selenabicyclo[3.3.1]nonanes // Molecules. – 2021. – V. 26. – Iss. 10. – ID:2849 (1-15). IF 4,412. DOI: 10.3390/molecules26102849
Musalov M.V., Potapov V.A., Yakimov V.A., Musalova M.V., Maylyan A.A., Zinchenko S.V., Amosova S.V. A Regioselective synthesis of novel functionalized organochalcogen compounds by chalcogenocyclofunctionalization reactions based on chalcogen halides and natural products // Molecules. – 2021. – V. 26. – Iss. 12. – ID:3729 (1-15). IF 4,412. DOI: 10.3390/molecules26123729
Amosova S.V., Shagun V.A., Makhaeva N.A., Novokshonova I.A., Potapov V.A. Quantum chemical and experimental studies of an unprecedented reaction pathway of nucleophilic substitution of 2-bromomethyl-1,3-thiaselenole with 1,3-benzothiazole-2-thiol proceeding stepwise at three different centers of seleniranium intermediates // Molecules. – 2021. – V. 26. – Iss. 21. – ID:6685 (1-16). IF 4,412. DOI: 10.3390/molecules26216685
Filippov A.S., Amosova S.V., Albanov A.I., Potapov V.A. Regioselective synthesis of novel functionalized dihydro-1,4- thiaselenin-2-ylsufanyl derivatives under phase transfer catalysis // Catalysts. – 2022. – V. 12. – Iss. 8. – Art. ID: 889 (1-15). IF 4,501. DOI: 10.3390/catal12080889
Potapov V.A., Musalov M.V. Triple-click chemistry of selenium dihalides: catalytic regioselective and highly efficient synthesis of bis-1,2,3-triazole derivatives of 9-selenabicyclo[3.3.1]nonane // Catalysts. – 2022. – V. 12. – Iss. 9.– ID:1032 (1-15). IF 4,501. DOI: 10.3390/catal12091032
Amosova S.V., Filippov A.S., Potapov V.A., Albanov A.I. Regio‐and stereoselective one-pot synthesis of new heterocyclic compounds with two selenium atoms based on 2-bromomethyl-1,3-thiaselenole using phase transfer catalysis // Catalysts. – 2022. – V. 12. – Iss. 10. – ID: 1236 (1-16). IF 4,501. DOI: 10.3390/catal12101236
Potapov V.A., Andreev M.V., Musalov M.V., Sterkhova I.V., Amosova S.V., Larina L.I. Regio and stereoselective synthesis of (Z,Z)-bis(3-amino-3-oxo-1-propenyl) selenides and diselenides based on 2-propynamides: a novel family of diselenides with high glutathione peroxidase-like activity // Inorganics. – 2022. – V. 10. – Iss. 6. – Art. ID: 74 (1-13). IF 3,149. DOI: 10.3390/inorganics10060074
Amosova S.V., Martynov A.V., Potapov V.A. 2-Bromomethyl-1,3-thiaselenole in click chemistry: synthesis of 1-(2,3-dihydro-1,4-thiaselenin-2-yl)-1H-1,2,3-triazoles via copper-catalyzed and thermal 1,3-dipolar cycloaddition with alkynes // Journal of Organometallic Chemistry. – 2022. – V. 977. – Art. ID: 122442 (1-8). IF 2,345. DOI: 10.1016/j.jorganchem.2022.122442
Musalov M.V., Potapov V.A., Maylyan A.A., Khabibulina A.G., Zinchenko S.V., Amosova S.V. Selenium dihalides click chemistry: highly efficient stereoselective addition to alkynes and evaluation of glutathione peroxidase-like activity of bis(E-2-halovinyl) selenides // Molecules. – 2022. – V. 27. – Iss. 3. – Art. ID: 1050 (1-13). IF 4,927. DOI: 10.3390/molecules27031050
Ogienko A.G., Nefedov A.A., Boldyrev V.V., Boldyreva E.V., Myz S.A., Voronkova O.M., Ogienko A.A., Adamova T.P., Amosova S.V., Trofimov B.A. Clathrate hydrates of organic solvents as auxiliary intermediates in pharmaceutical research and development: improving dissolution behaviour of a new anti-tuberculosis drug, Perchlozon // Pharmaceutics. – 2022. – V. 14. – Iss. 3. – Art. ID: 495 (1-17). IF 6,525. DOI: 10.3390/pharmaceutics14030495
Filippov A.S., Amosova S.V., Makhaeva N.A., Albanov A.I., Potapov V.A. Efficient regioselective synthesis of novel ensembles of organylselanyl-functionalized divinyl sulfides and 1,3-thiaselenoles under phase transfer catalysis conditions // Catalysts. – 2023. – V. 13. – Iss. 8. – ID:1227 (1-13). IF 3,9 DOI: 10.3390/catal13081227
Andreev M.V., Potapov V.A., Musalov M.V., Larina L.I. A new family of vinyl selenocyanates with the amide function based on the reaction of potassium selenocyanate with 3-trimethylsilyl-2-propynamides // Catalysts. – 2023. – V. 13. – Iss. 9. – ID:1257 (1-16). DOI: 10.3390/catal13091257
Andreev M.V., Potapov V.A., Musalov M.V., Larina L.I. First examples of reactions of 3-trimethylsilyl-2-propynamides and organic diselenides: synthesis of novel derivatives of propynamides // Catalysts. – 2023. – V. 13. – Iss. 10. – ID:1326 (1-15). IF 3,9. DOI: 10.3390/catal13101326
Amosova S.V., Filippov A.S., Makhaeva N.A., Albanov A.I., Potapov V.A. Green organoselenium chemistry: selective syntheses of new 1,4-thiaselenine derivatives based on reactions of thiaselenole reagent with alcohols and water // Inorganics. – 2023. – V.11. – Iss. 7. – ID:281 (1-18). IF 2,9. DOI: 10.3390/inorganics11070281
Musalov M.V., Kapustina I.S., Spiridonova E.V., Ozolina N.V., Amosova S.V., Borodina T.N., Potapov V.A. Transannular selenocyclofunctionalization of 1,5-cyclooctadiene: the antioxidant properties of 9-selenabicyclo[3.3.1]nonane derivatives and the discovery of increasing both GPx and GR activities // Inorganics. – 2023. – V.11. – Iss. 7. – ID: 304 (1-15). IF 2,9. DOI: 10.3390/inorganics11070304
Musalov M.V., Amosova S.V., Potapov V.A. Selenium dibromide click chemistry: the efficient synthesis of novel selenabicyclo[3.3.1]nonene-2 and -nonane derivatives // International Journal of Molecular Sciences. – 2023. – V. 24. – Iss. 24. – ID:17485 (1-23). IF 5,6. DOI: 10.3390/ijms242417485
Amosova S.V., Filippov A.S., Makhaeva N.A., Albanov A.I., Potapov V.A. Polyunsaturated sulfur/selenium-containing products based on regio- and stereoselective nucleophilic addition and substitution reactions of 1,2-bis[(Z)-2-(vinylsulfanyl)ethenyl] diselane // New Journal of Chemistry. – 2023. – V. 47. – Iss. 24. – P. 11505-11514. IF 3,3. DOI: 10.1039/d3nj01147j
Musalov M.V. New chemo-, regio- and stereoselective reactions and methods in organic synthesis // International Journal of Molecular Sciences. – 2024. – V. 25. – Iss. 24. – ID: 13409 (1-17). IF: 4,9. DOI: 10.3390/ijms252413409
Potapov V.A., Novokshonova I.A., Musalov M.V., Amosova S.V., Rakitin O.A. Methyl 6,7-difluoro-2-[(4-fluorobenzyl)sulfanyl]-4-hydroxyquinoline-3-carboxylate // Molbank. – 2024. – V. 2024. – Iss. 4. – ID:M1889 (1-6). DOI: 10.3390/M1889
Andreev M.V. DABCO-Catalyzed tandem Si-Csp-desilylation-addition reactions of 3-trimethylsilyl-2-propynamides with acetylenic alcohols and diols: synthesis of β-(Propargyloxy)acrylamides // Journal of Organometallic Chemistry. – 2024. – V. 1017. – ID:123289 (1-10). IF: 2,1. DOI: 10.1016/j.jorganchem.2024.123289
A. Potapov, R.S. Ishigeev, L.A. Belovezhets, S.V. Amosova. Novel Family of Selenazolo[3,2-a]pyridinium Derivatives Based on Annulation Reactions and Comparative Analysis of Antimicrobial Activity of the Selenium and Sulfur Analogs of Chalcogenazolo[3,2-a]pyridiniums. Curr. Org. Chem.2025, vol. 29, p. 669-678. DOI: 10.2174/0113852728326804240828071148
Статьи в отечественных журналах за 5 лет (2021-2025)
Потапов В.А., Хабибулина А.Г., Мусалова М.В., Мусалов М.В., Шкурченко И.В., АлбановА.И., Амосова С.В. Эффективный синтез алкил(2,3-дигидро-1-бензофуран-2-илметил)телланов на базе тетрагалогенидов теллура и 2-аллилфенолов // Журнал органической химии. – 2021. – Т. 57. – N – С. 524-531. DOI: 10.1134/S1070428021040072
Мусалов М.В., Якимов В.А., Потапов В.А., Зинченко С.В., Амосова С.В. Однореакторные методы синтеза функциональных дигидробензоселенофенов и селенохроманов из ацетилэвгенола и дибромида селена. Перегруппировка 2-бромметил-2,3-дигидробензоселенофена в селенохроманы // Журнал органической химии. – 2021. – Т. 57. – N – С. 541-549. DOI: 10.1134/S1070428021040096
Мусалов М.В., Живетьева С.А., Потапов В.А., Амосова С.В. Однореакторный синтез функциональных 2,6-дипиридиноний-9-селенабицикло[3.3.1]нонанов // Журнал органической химии. – 2021. – Т. 57. – N – С. 588-591. DOI: 10.1134/S1070428021040254
Мартынов А.В., Махаева Н.А., Мусалов М.В., Амосова С.В. Кросс-сочетание бис(E-2-бромвинил)селенида с терминальными ацетиленами в присутствии PD(PPH3)4: первый пример вовлечения винилселенидов в реакцию Соногаширы // Журнал органической химии. – 2021. – Т. 57. – N – С.1641-1646. DOI: 10.1134/S1070428021110117
Мусалов М.В., Майлян А.А., Мусалова М.В., Амосова С.В., Потапов В.А. Стереоселективный синтез функциональных дивинилсульфидов на основе дихлорида серы и (триметилсилил)ацетилена // Известия Академии наук. Серия химическая. – 2021. – N 2. – С. 420-423. DOI: 10.1007/s11172-021-3102-x
Дубровина В.И., Старовойтова Т.П., Юрьева О.В., Пятидесятникова А.Б., Потапов В.А., Мусалов М.В., Балахонов С.В. Влияние синтетического селеноорганического соединения на поствакцинальный иммунопоэз в красном костном мозге и клеточный состав периферической крови белых мышей, вакцинированныхYersinia pestis EV // Бюллетень экспериментальной биологии и медицины. – 2021. – Т. 171. – N – С. 628-632. DOI: 10.1007/s10517-021-05287-0
Андреев М.В., Демина М.М., Медведева А.С., Сафронова Л.П., Албанов А.И., Афонин А.В. Синтез 3-хлор-3-триметилсилил-2-пропенамидов и гидразидов на основе 3-триметилсилилпропиоловой кислоты // Журнал органической химии. – 2021. – Т. 57. – N – С.550-561. DOI: 10.1134/S1070428021040102
Ишигеев Р.С., Амосова С.В., Потапов В.А. Региоселективные реакции пиридин-2-сульфенилбромида с виниловыми и аллиловыми эфирами // Журнал общей химии. – 2022. – Т. 92. – N 9. – С. 1480-1488. DOI: 10.31857/S0044460X22090141
Мусалов М.В., Живетьева С.А., Шкурченко И.В., Амосова С.В., Потапов В.А. Синтез пиридиниевых солей 2,6-дибром-9-селенабицикло[3.3.1]нонана, содержащих ацетальные группы // Журнал органической химии. – 2022. – Т. 58. – N 4. – С. 430-435. DOI: 10.31857/S0514749222040085
IshigeevR.S., Amosova S.V., Potapov V.A. Regioselective synthesis of new [1,3]thiazolo and [1,3]selenazolo[3,2-a]pyridinium derivatives // Russian Journal of General Chemistry. – 2023. – V. 93. – Suppl. Iss. 1. – P. S87-S DOI: 10.1134/S1070363223140360
Пятидесятникова А.Б., Дубровина В.И., Юрьева О.В., Корытов К.М., Иванова Т.А., ПотаповВ.А., Мусалов М.В., Балахонов С.В. Влияние селенорганического соединения 974zh на экспрессию генов TLR2 и TLR4 в клетках крови и селезёнки экспериментальных животных при совместном введении с Yersinia pestis EV // Acta biomedica scientifica. – 2024. – Т. 9. – N – С. 249-255. DOI: 10.29413/ABS.2024-9.3.25
Ишигеев Р.С., Амосова С.В., Потапов В.А. Реакция пиримидин-2-сульфенилхлорида с алкилвиниловыми и аллиловыми эфирами // Журнал общей химии. – 2024. – Т. 94. – N 7. – С. 836-842. DOI: 10.31857/S0044460X24070058
Ишигеев Р.С., Хабибулина А.Г., Потапов В.А. Синтез новых производных халькогеназоло[3,2-a]пиридиния реакцией аннелирования винилгетероатомных соединений пиридин-2-халькогенилгалогенидами // Журнал общей химии. – 2024. – Т. 94. – N – С.949-957. DOI: 10.31857/S0044460X24090018
Хабибулина А.Г. Эффективный метод синтеза 3,5-бис(сульфанилметил)-1,4-оксаселенанов // Журнал общей химии. – 2024. – Т. 94. – N 10. – С. 1014-1020. DOI: 10.31857/S0044460X24100014.
Ишигеев Р.С., Хабибулина А.Г. Региоселективный синтез новых конденсированных соединений на основе пиридин-2-халькогенилгалогенидов, 1-алкенов и арилалкенов // Журнал общей химии. – 2024. – Т. 94. – N 11-12. – C. 1086-1094. DOI: 10.31857/S0044460X24110032
BelyakovaYu.Yu., Yaremenko I. A., Terent’ev A. O., …, Musalov M.V., Amosova S.V., Potapov V.A., et al. Russian Journal of General Chemistry. 2026. Vol. 96. P. 1. DOI: 10.1134/S1070363225605721
Makhaeva N.A., Potapov V.A. New aspects of the chemistry of thiomorpholines // Russian Journal of Organic Chemistry. – 2025. –Vol. 61, No. 12. – P. 2247-2258.
Ishigeev R.S., Potapov V.A. New condensed chalcogen-nitrogen-containing compounds based on reactions of hetarenchalcogenyl halides with pentene // Russian Journal of Organic Chemistry. – 2025. – Vol. 61, No. 12. – P. 2267-2275.
Ishigeev R.S., Zhivetyeva S.A., Potapov V.A. Synthesis of new functional compounds based on bis(1,3-benzothiazol-2-yl) disulfide and unsaturated hydrocarbons // Russian Journal of Organic Chemistry. – 2025. – Vol. 61, No. 12. – Р. 2259-2266.
Musalova M.V., Musalov M.V., Pakeeva A.A., Ivanova L.A., Potapov V.A.Synthesis of Novel Bifunctional Organochalcogen Compounds by Reactions of Tellurium, Selenium and Sulfur Halides with Allylacetic Acid // Russian Journal of Organic Chemistry. – 2025. – Vol. 61, No. 11. – P. 2104-2110. DOI: 1134/S1070428025604881
MusalovM.V., Pakeeva A.A., Potapov V.A. Synthesis of New Derivatives of 9-Selenabicyclo[4.2.1]nonane by the Transannular Addition of Selenium Dihalides to 1,3-Cyclooctadiene // Russian Journal of Organic Chemistry. – 2025. – Vol. 61, No. 11. – P. 2097-2103. DOI: 1134/S1070428025604789
Andreev M.V., Potapov V.A., Musalov M.V., Larina L.I. Regio- and Stereoselective Synthesis of New (Z)-Selenocyanatoacrylamides // Russian Journal of Organic Chemistry. – 2025. – Vol. 61, No. 11. – P. 2111-2123. DOI: 1134/S1070428025605114
Мусалов М. В., Пакеева А. А., Потапов В. А. Однореакторный метод синтеза 2,6-бис(органилсульфанил)-9-селенабицикло[3.3.1]нонанов из дибромида селена, циклооктадиена и тиолов // Журнал общей химии. – 2025. – Т. 95, № 11-12. – С. 572-578. DOI: 7868/S3034559625110128
Филиппов А. С. Синтез новых производных 2,3-дигидро-1,4-тиаселенина реакцией 2-бромметил-1,3-тиаселенола с карбоновыми и дикарбоновыми кислотами и их солями // Журнал общей химии. – 2025. – Т. 95, № 11-12. – С. 562-571. DOI: 7868/S3034559625110117