Руководитель

Кадровый состав
Петрова Ольга Витальевна – к.х.н., с.н.с.
Сагитова Елена Фаритовна – к.х.н., с.н.с.
Щербакова Виктория Сергеевна – к.х.н., с.н.с.
Мартыновская Светлана Валерьевна – к.х.н., с.н.с.
Будаев Арсалан Бадмаевич – к.х.н., н.с.
Гыргенова Елена Андреевна – м.н.с.
Степанова Софья Александровна – м.н.с.
Макаренко Даниил Алексеевич – лаборант
6. Синтез ранее неизвестных гетероциклических ансамблей и конденсированных соединений на платформе 2-ацилэтинилпирролов
6.1. На основе реакций ставших легко доступными 2-ацилэтинилпирролов с С-нуклеофилами (ацетонитрил, малононитрил, метиленоактивные эфиры и амиды, тозилметилизоцианид) разработаны новые, эффективные методы синтеза ранее неизвестных пирролсодержащих гетероциклических ансамблей – пирролил-пиридинов, пирролил-дицианоанилинов, пирролил-пиронов, пирролил-аминопиронов, пирролил-пиридонов, и бипирролов, а также функционализированных ацильными и тозильной группами С-винилпирролов и тозилпирролил-1,3-енинов.
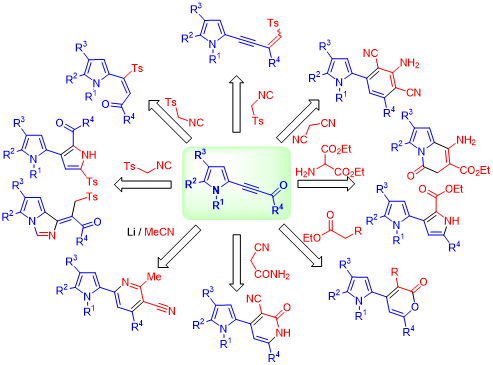
Gotsko, M.D., Saliy, I.V., Ushakov, I.A., Sobenina, L.N., Trofimov, B.A. Functionalized 2,3′-Bipyrroles and Pyrrolo[1,2-c]imidazoles from Acylethynylpyrroles and Tosylmethylisocyanide // Molecules 2024. – 29. – 885. DOI: 10.3390/molecules29040885D.
Gotsko, I. V. Saliy, I. A. Ushakov, L. N. Sobenina, B. A. Trofimov, One-pot synthesis of functionalized dihydroindolizinones from pyrrolylpropynoates and diethyl aminomalonate // Mendeleev Commun. – 2025. – 35. –1. – 99. DOI: 10.71267/mencom.7547
Gotsko M.D., Saliy I.V., Sobenina L.N., Ushakov I.A., Trofimov B.A. From acylethynylpyrroles to pyrrole-pyrone ensembles in a one step // Tetrahedron Letters. – 2019. – V. 60. – № 151126., DOI: 10.1016/j.tetlet.2019.151126.
Saliy I.V., Gotsko M.D., Sobenina L.N., Ushakov I.A., Trofimov B.A. Bio-inspired functionalized pyrrole-pyridone ensembles: synthesis on the platform of acylethynylpyrroles // Synthesis. – 2020. – V. 52. – N. 18. – P. 2698-2704. DOI: 10.1055/s-0040-1707148.
Saliy I.V., Gotsko M.D., Sobenina L.N., Ushakov I.A., Trofimov B.A. Chemo- and stereoselective synthesis of E-2-(2-acyl-1-tosylvinyl)pyrroles from tosylmethyl isocyanide (TosMIC) and 2-(acylethynyl)pyrroles // Tetrahedron Letters. – 2021. – V. 84. – № 153432. DOI: 10.1016/j.tetlet.2021.153432.
Trofimov B.A., Gotsko M.D., Saliy I.V., Sobenina L.N., , Ushakov I.A., Kireeva V.V. Functionalized Bipyrroles and Pyrrolyl-Aminopyrones from Acylethynylpyrroles and Diethyl Aminomalonate. // Synthesis. – 2021. – V. 54. –– P. 1134-1144. DOI:10.1055/a-1681-4164.
Gotsko M.D., Saliy, I.V., Ushakov I.A., Sobenina L.N.,, Trofimov B.A. Substituent-Dependent Divergent Synthesis of 2-(3-Amino-2,4-dicyanophenyl)pyrroles, Pyrrolyldienols and 3-Amino-1-acylethylidene-2-cyanopyrrolizines via Reaction of Acylethynylpyrroles with Malononitrile // Molecules. – 2022. –V. 27. – №. 8528. DOI: 10.3390/molecules27238528.
Tomilin D.N., Sobenina L.N., Saliy I.V., Ushakov I.A., Belogolova A.M., Trofimov B.A. Substituted pyrrolyl-cyanopyridines on the platform of acylethynylpyrroles via their 1 : 2 annulation with acetonitrile under the action of lithium metal // New Journal of Chemistry. – 2022. – V. 46. – N. 27. – P. 13149-13155. DOI: 10.1039/D2NJ02011D.
Gotsko M.D., Saliy I.V., Sobenina L.N., Ushakov I.A., Trofimov B.A. Tosyl/pyrrolyl-capped 1,3-enynes via t-BuOK-assisted reaction of TosMIC with acylethynylpyrroles: a new feature of this popular reagent // New Journal of Chemistry. – 2022. – V. 46. – N. 35. – P. 16646-16650. DOI: 10.1039/D2NJ02827A.
6.2 На основе реакции 2-ацилэтинилпирролов с N-нуклеофилами разработаны эффективные методы синтеза функционализированных линейно связанных и конденсированных пиррольных систем, таких как бипирролы, пирролил-пиридины, пирролил-пиразолы, пирролил-изоксазолы, пирролил-имидазолины, пирролопиразины, пирролизины и пирролоксазолы. Ряд синтезированных пиррольных структур проявляют значительную ингибирующую активность ферментов ацетилхолинэстеразы и α-гликозидазы, что делает их кандидатами в противодиабетические препараты и препараты для лечения болезни Альцгеймера.
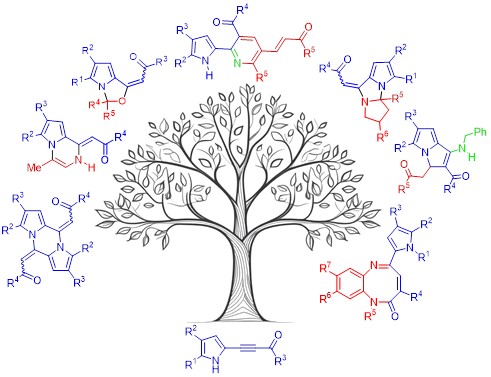
Petrova O.V., Tomilin D.N., Şenol H., Belyaeva K.V., Nikitina L.P., Oparina L.A., Sobenina L.N., Trofimov B.A., Sadeghian N., Taslimi P., Farzaliyev V., Sujayev A., Gulçin İ. / Synthesis of pyrrole-heterocyclic derivatives as anti-Alzheimer and antidiabetic candidates: An in vitro-in silico study // J. Mol. Struct. – 2024. – V.1315. – P.138998. DOI: 10.1016/j.molstruc.2024.138998
Tomilin D.N., Stepanova S.A., Sobenina L.N., Ushakov I.A., Trofimov B.A. / Acylmethylidenepyrrolo[1,2-c]oxazoles via [3+2]-cyclization of 2-acylethynylpyrroles with carbonyl compounds // New J. Chem. – 2023.– V.47. – P. 17810. DOI: 10.1039/d3nj03142j
Sobenina L.N., Tomilin D.N., Sagitova E.F., Ushakov I.A., Trofimov B.A. Transition metal-free, atom- and step-economic synthesis of aminoketopyrrolizines from benzylamine, acylethynylpyrroles and acylacetylenes // Org. Lett. – 2017. – V. 19, No 7. – P. 1586-1589. DOI: 10.1021/acs.orglett.7b00408.
Sobenina L.N., Sagitova E.F., Ushakov I.A., Trofimov B.A. Transition-metal-free synthesis of pyrrolo[1,2-a]pyrazines via intramolecular cyclization of N-propargyl(pyrrolyl)enaminones // Synthesis. – 2017. – V. 49, No 17. – P. 4065-4081. Имп. Факт. 2.650. DOI: 10.1055/s-0036-1588454.
Tomilin D. N., Sobenina L. N., Ushakov I. A., Trofimov B. A. Highly functionalized pyrrolylpyridines from 2-(acylethynyl)pyrroles // Synthesis. – 2021. – V. 53. – Iss. 6. – P. 1137-1148. DOI: 10.1055/s-0040-1706474.
7. Стереоселективный синтез гибридов пирроло[1,2-c]тиазолов с винилкетонами из 2-ацилэтинилпирролов и сероуглерода
На основе доступных 2-ацилэтинилпирролов созданы подходы к новым сераорганическим соединениям. Разработана атомэкономная стратегия управляемого синтеза пирроло[1,2-c]тиазол-3-тионов и спироби[пирроло[1,2-c]тиазолов], в том числе индольного ряда. Переключение направлений сборки пирроло[1,2-c]тиазол-3-тионов либо спироби[пирроло[1,2-c]тиазолов] достигается изменением соотношения реагентов и заместителями в пиррольном кольце. Все варианты [3+2]-циклизации строго стереоселективны: образуются только аддукты Z-конфигурации α,β-этиленовых групп.
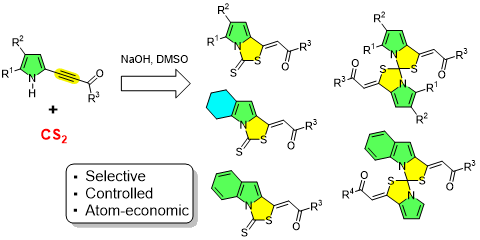
Tomilin D.N., Stepanova S.A., Ushakov I.A., Vashchenko A.V., Trofimov B.A. / Controlled Switching from Spirobi[pyrrolo[1,2-c]thiazoles] to Pyrrolo[1,2-c]thiazole-3-thiones during the Cyclization of 2-Acylethynylpyrroles with Carbon Disulfide // J. Org. Chem. – 2025. – V.90. – N.30. – P.10919–10926. DOI: 10.1021/acs.joc.5c00719
Tomilin D.N., Stepanova S.A., Borodina T.N., Ushakov I.A., Trofimov B.A. / Synthesis of functionalized thiazoloindole-3-thiones and their spirocongeners from 2-acylethynyl-4,5,6,7-tetrahydroindoles and carbon disulfide // New J. Chem. – 2025. – V.49. – P.16820–16827. DOI: 10.1039/D5NJ02380G
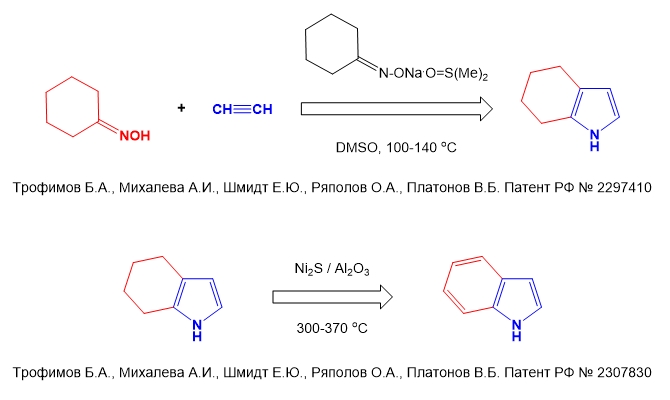
8. Промышленно-ориентированная технология синтеза 4,5,6,7-тетерагидроиндола и индола из циклогексаноноксима (планшет 3)
Разработаны ориентированные на промышленность технологии синтеза 4,5,6,7-тетрагидроиндола из циклогексаноноксима и ацетилена с использованием в качестве катализатора системы циклогексаноноксимат натрия/ДМСО и селективного метода дегидрирования 4,5,6,7-тетерагидроиндола в индол с использованием системы Ni2S/γ-Al2O3 в качестве катализатора (совместно с компанией Waldis, Литва).
9. Разработка метода получения перспективного класса строительных блоков – N-алленилпиррол-2-карбальдегидов
Разработан способ селективного получения ранее неизвестного класса N-алленилпиррол-2-карбальдегидов последовательным пропаргилированием замещенных NH-пирролов в суперосновной системе KOH/ДМСО и введением в полученные N-алленилпирролы формильной группы с помощью модифицированной реакции Вильсмайeра-Хаака. Полученные соединения являются перспективными строительными блоками для тонкого органического синтеза.
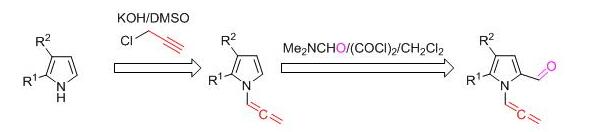
Martynovskaya S.V. , Shcherbakova V.S., Ushakov I.A., Borodina T.N., Ivanov A.V. / Expedient synthesis of a new class of organic building blocks: N-allenylpyrrole-2-carbaldehydes // Tetrahedron Letters. – 2020. – V. 61. – 152666. DOI: 10.1016/j.tetlet.2020.152666.
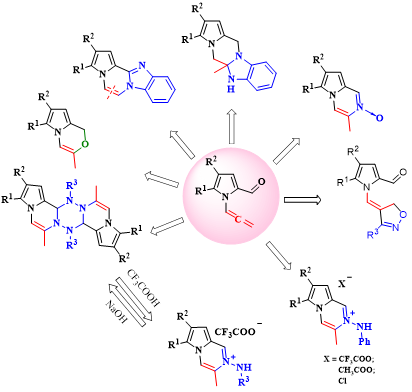
10. N-Алленилпиррол-2-карбальдегиды как универсальная платформа для создания широкой библиотеки новых аннелированных пирролсодержащих гетероциклических систем
На основе реакции N-алленилпиррол-2-карбальдегида, как универсального строительного блока в органическом синтезе, и разнообразных нуклеофилов (гидроксиламин, о-фенилендиамин, нитрилоксид, гидразин и его производные) разработаны эффективные методологии синтеза аннелированных азотсодержащих гетероциклических ансамблей, таких как пирролопиразин-N-оксиды, бензимидазопирролопиразины, дигидробензимидазопирролопиразины, пирролооксазины, тетрагидродипирролодипиразинотетразины, соли N-аминопирроло[1,2-a]пиразиния, 1,2-оксазолиновые пирролкарбальдегиды.
.
Ivanov A.V., Martynovskaya S.V., Shcherbakova V.S., Ushakov I.A., Borodina T.N., Bobkov A.S, Vitkovskaya N.M. / Ambient access to a new family of pyrrole-fused pyrazine nitrones via 2-carbonyl-N-allenylpyrroles // Org. Chem. Front. – 2020. – V.7. – P.4019–4025. DOI: 10.1039/D0QO00762E
Vitkovskaya N.M., Bobkov A.S., Kuznetsova S.V., Shcherbakova V.S., Ivanov A.V. / Base-Promoted Formation of Annelated Pyrrolo-1,4-oxazine Ensemble from 1H-pyrrol-2-ylmethanol and Propargyl Chloride // ChemPlusChem. – 2020. – V.84. – P.88–100. DOI: 10.1002/cplu.201900407
Martynovskaya S.V., Budaev A.B., Ushakov I.A., Borodina T.N., Ivanov A.V. / Solvent Moisture-Controlled Self-Assembly of Fused Benzoimidazopyrrolopyrazines with Different Ring’s Interposition // Molecules. – 2022. – V.27. – P.2460. DOI: 10.3390/molecules27082460
Ivanov A.V., Bobkov A.S., Martynovskaya S.V., Budaev A.B., Vitkovskaya N.M. / A Short-Cut to Substituted Fused Pyrrolo[2,1-c][1,4]oxazines: A Hybrid Theoretical and Experimental Study // Asian J. Org. Chem. – 2023. – e202300153. DOI: 10.1002/ajoc.202300153
Martynovskaya S.V., Gyrgenova E.A., Ushakov I.A., Borodina T.N., Ivanov A.V. / Synthesis of Tetrazines from N-Allenylpyrrole-2-carbaldehydes and pH-Controlled Reversible Fragmentation // Org.Lett. – 2024. – V.26. – P.132−136. DOI: 10.1021/acs.orglett.3c03751
Ivanova E.E., Martynovskaya S.V., Ushakov I.A., Vashchenko A.V., Bobkov A.S., Teplyashin N.V., Vitovskaya O.P., Ivanov A.V. / Double Selectivity of Cycloaddition Opens a Way to 1,2-Oxazoline-Pyrrole Ensembles via Nitrile Oxide Cycloaddition to N-Allenylpyrrole-2-Carbaldehydes // J. Org. Chem. – 2025. – V.90. – P.8507−8518. DOI: 10.1021/acs.joc.5c00372
Bobkov A.S., Teplyashin N.V., Martynovskaya S.V., Ivanov A.V., Vitkovskaya N.M. / Reaction of N-Allenyl-1H-Pyrrole-2-Yl-Carbaldehydes With Hydroxylamine: A Quantum Chemical Insight Into the Mechanism and Substituent Influence // J. Phys. Org. Chem. – 2025. – 38:e70023. DOI: 10.1002/poc.70023
Gyrgenova E.A., Martynovskaya S.V., Ushakov I.A., Ivanov A.V. / Assembly of phenylaminopyrrolo[1,2-a]pyrazinium salts from N-allenylpyrrole-2-carbaldehydes and phenylhydrazine in the presence of acids // Russ. Chem. Bull. – 2025. – V.74. –N.1. – P.143–150. DOI: 10.1007/s11172-025-4510-0
Gyrgenova E.A., Petrushenko K.B., Shcherbakova V.S., Ivanov A.V. / Colorimetric and fluorescent pH-probe based on the reversible fragmentation of tetrahydrodipyrrolodipyrazinotetrazine derivatives // Dyes and Pigments. – 2026. – V.247. – P.113510. DOI:10.1016/j.dyepig.2025.113510
Гранты, контракты, хоздоговора, партнеры по инновационным исследованиям за последние 3 года
Грант РНФ 21-73-10134 «Разработка общей однореакторной и атом-экономной методологии построения пирроло-имидазолидиновых структур на основе новой реакции циклоприсоединения пирролилацетиленов к двойной С=N связи» (руководитель д.х.н Беляева К.В.)
Грант РФФИ 20-33-90187 «С-Ацилэтинилпирролы в дизайне функционализированных пиррольных систем – перспективных лекарственных средств и их прекурсоров» (руководитель д.х.н. Л.Н. Собенина)
Грант РНФ 19-73-10063 «Пирролы с электронодефицитными ацетиленовыми заместителями как платформа для построения поляризованных дипиррометанов/дипиррометенов и борфторидных хелатных комплексов на их основе – новых флуорофоров и красителей медицинского назначения, прекурсоров антибактериальных и онкоориентированных лекарств, компонентов оптоэлектронных материалов» (руководитель к.х.н. Д.Н. Томилин)
Грант РФФИ-Государственный фонд естественных наук Китая 19-53-53008 «Создание новых флуоресцентных сенсоров типа BODIPY, обладающих повышенной чувствительностью к изменениям в биологических объектах и окружающей среде» (руководитель академик РАН Б.А. Трофимов)
Грант РФФИ 19-33-90051 «N-Алленилпиррол-2-карбальдегиды как универсальная платформа для создания широкой библиотеки новых аннелированных пирролсодержащих гетероциклических систем» (руководитель д.х.н Иванов А.В.)
Награды
Томилин Денис Николаевич – именная стипендия Фонда Стратегического и Инновационного Развития Иркутской Области, 2022 год
Щербакова Виктория Сергеевна – лауреат конкурса в сфере науки и техники 2022 года, диплом за разработку технологии получения востребованных виниловых эфиров путем утилизации хлорорганических отходов
Мартыновская Светлана Валерьевна – стипендия Губернатора Иркутской Области, 2019 год
Мартыновская Светлана Валерьевна – лауреат Конкурса проектов молодых ученых 2021 года, диплом 1 степени
Мартыновская Светлана Валерьевна – лауреат конкурса в сфере науки и техники 2022 года, диплом за разработку технологии получения востребованных виниловых эфиров путем утилизации хлорорганических отходов
Мартыновская Светлана Валерьевна – именная стипендия Фонда Стратегического и Инновационного Развития Иркутской Области, 2022 год
Гыргенова Елена Андреевна – диплом за лучший стендовый доклад на конференции «Фаворский 2023»
Гыргенова Елена Андреевна – именная стипендия Фонда Стратегического и Инновационного Развития Иркутской Области, 2024 год
Избранные публикации за последние 3 года
Обзоры
Иванов А.В., Щербакова В.С., Собенина Л.Н. / Замещенные пирролы на основе кетонов: перспективы использования и достижения в синтезе // Успехи химии. – 2023. – T.92. – N.9. – RCR5090. DOI: 10.59761/RCR5090
Собенина Л.Н., Томилин Д.Н. / Синтез и перспективы применения мезо-CF3-флуорофоров BODIPY // Журнал Общей Химии. – 2024. –T.93. – C.143–172. DOI: 10.1134/S1070363223140050
Чарушин В.Н., Вербицкий Е.В., Чупахин О.Н., Воробьева Д.В., Грибанов П.С., Осипов С.Н., Иванов А.В., Мартыновская С.В., Сагитова Е.Ф., Дяченко В.Д., Дяченко И.В., Кривоколыско С.Г., Доценко В.В., Аксенов А.В., Аксенов Д.А., Аксенов Н.А., Ларин А.А., Ферштат Л.Л., Музалевский В.М., Ненайденко В.Г., Гулевская А.В., Пожарский А.Ф., Филатова Е.А., Беляева К.В., Трофимов Б.А., Балова И.А., Данилкина Н.А., Говди А.И., Тихомиров А.С., Щекотихин А.Е., Новиков М.С., Ростовский Н.В., Хлебников А.Ф., Климочкин Ю.Н., Леонова М.В., Ткаченко И.М., Мамедов В.А., Мамедова В.Л., Жукова Н.А., Семёнов В.Э., Синяшин О.Г., Борщев О.В., Лупоносов Ю.Н., Пономаренко С.А., Фисюк А.С., Костюченко А.С., Илькин В.Г., Березкина Т.В., Бакулев В.А., Газизов А.С., Загидуллин А.А., Карасик А.А., Кукушкин М.Е., Белоглазкина Е.К., Голанцов Н.Е., Феста А.А., Воскресенский Л.Г., Мошкин В.С., Буев Е.М., Сосновских В.Я., Миронова И.А., Постников П.С., Жданкин В.В., Юсубов М.С., Ярёменко И.А., Виль В.А., Крылов И.Б., Терентьев А.О., Горбунова Ю.Г., Мартынов А.Г., Цивадзе А.Ю., Стужин П.А., Иванова С.С., Койфман О.И., Буров О.Н., Клецкий М.Е., Курбатов С.В., Яровая О.И., Волчо К.П., Салахутдинов Н.Ф., Панова М.А., Бургарт Я.В., Салоутин В.И., Ситдикова А.Р., Щегравина Е.С., Федоров А.Ю. / Успехи в химии гетероциклических соединений в 21 веке // Успехи химии. – 2024. – Т.93. – N.7. – RCR DOI:10.59761/RCR5125
Gyrgenova E.A., Titova Y.Y., Ivanov A.V. / Efficient Approaches to the Design of Six-Membered Polyazacyclic Compounds—Part 1: Aromatic Frameworks // Molecules. – 2025. – V.30. – N.15. – 3264. DOI:3390/molecules30153264
Titova YU.YU., Gyrgenova E.A., Ivanov A.V. Efficient Approaches to the Design of Six-Membered Polyazacyclic Compounds—Part 2: Nonaromatic Frameworks // Molecules. – 2025. – V.30. – N.19. – 3911. DOI:3390/molecules30193911
Статьи
Tomilin D.N., Stepanova S.A., Sobenina L.N., Ushakov I.A., Trofimov B.A. / Acylmethylidenepyrrolo[1,2-c]oxazoles via [3+2]-cyclization of 2-acylethynylpyrroles with carbonyl compounds // New J. Chem. –2023. –47. – P.17810. DOI: 10.1039/d3nj03142j
Ivanov A.V., Bobkov A.S., Martynovskaya S.V., Budaev A.B., Vitkovskaya N.M. / A Short-Cut to Substituted Fused Pyrrolo[2,1-c][1,4]oxazines: A Hybrid Theoretical and Experimental Study // Asian J. Org. Chem. – 2023. – e202300153.
Trofimov B.A., Sobenina L.N., Petrova O.V., Sagitova E.F., Petrushenko K.B., Tomilin D.N., Martyanova E.G., Razumov V.F., Oparina L.A., Ushakov I.A., Korchagin D.V., Belogolova A.M., Trofimov A.B. Macrocyclic bridgehead fluorophores, pyrrolyl-diazabicyclo [8.3.1]-tetradecadienones, with giant stokes shifts // Org. Chem.– 2024. – V.89. – N.24. – P.18142–18158. DOI: 10.1021/acs.joc.4c02002
Martynovskaya S.V., Gyrgenova E.A., Ushakov I.A., Borodina T.N., Ivanov A.V. Synthesis of Tetrazines from N-Allenylpyrrole-2-carbaldehydes and pH-Controlled Reversible Fragmentation // Lett. – 2024. – V.26. – N.1. – P.132–136. DOI: 10.1021/acs.orglett.3c03751
Tomilin D.N., Stepanova S.A., Ushakov I.A., Vashchenko A.V., Trofimov B.A. /Controlled Switching from Spirobi[pyrrolo[1,2-c]thiazoles] to Pyrrolo[1,2-c]thiazole-3-thiones during the Cyclization of 2-Acylethynylpyrroles with Carbon Disulfide // Org. Chem. – 2025. – V.90. – N.30. – P.10919–10926. DOI: 10.1021/acs.joc.5c00719
Tomilin D.N., Stepanova S.A., Borodina T.N., Ushakov I.A., Trofimov B.A. / Synthesis of functionalized thiazoloindole-3-thiones and their spirocongeners from 2-acylethynyl-4,5,6,7-tetrahydroindoles and carbon disulfide // New J. Chem. –2025. –49. – P.16820–16827. DOI: 10.1039/D5NJ02380G
Ivanova E.E., Martynovskaya S.V., Ushakov I.A., Vashchenko A.V., Bobkov A.S., Teplyashin N.V., Vitovskaya O.P., Ivanov A.V. / Double Selectivity of Cycloaddition Opens a Way to 1,2-Oxazoline-Pyrrole Ensembles via Nitrile Oxide Cycloaddition to N-Allenylpyrrole-2-Carbaldehydes // J. Org. Chem. – 2025. – V.90. – 8507-8518. DOI: 10.1021/acs.joc.5c00372
Gyrgenova E.A., Petrushenko K.B., Shcherbakova V.S., Ivanov A.V. / Colorimetric and fluorescent pH-probe based on the reversible fragmentation of tetrahydrodipyrrolodipyrazinotetrazine derivatives // Dyes and Pigments. – 2026. – V. 247. – P.113510. DOI:10.1016/j.dyepig.2025.113510
Bobkov A.S., Teplyashin N.V., Martynovskaya S.V., Ivanov A.V., Vitkovskaya N.M. / Reaction of N-Allenyl-1H-Pyrrole-2-Yl-Carbaldehydes With Hydroxylamine: A Quantum Chemical Insight Into the Mechanism and Substituent Influence // J. Phys. Org. – 2025. – 38:e70023. DOI: 10.1002/poc.70023
Gyrgenova E.A., Martynovskaya S.V., Ushakov I.A., Ivanov A.V. / Assembly of phenylaminopyrrolo[1,2-a]pyrazinium salts from N-allenylpyrrole-2-carbaldehydes and phenylhydrazine in the presence of acids // Russ. Chem. Bull. – 2025. – V.74. – N.1. – P.143–150. DOI: 10.1007/s11172-025-4510-0
Обложки в научных журналах















